题目内容
11.以下的说法中错误的是( )| A. | 无论乙烯的加成,还是乙烷的取代反应都可制得溴乙烷 | |
| B. | 无论使用溴水或KMnO4溶液都可以鉴别乙烯和乙烷 | |
| C. | 相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同 | |
| D. | 乙烯的化学性质比乙烷的化学性质活泼 |
分析 A.乙烯与HBr发生加成反应的产物只有一种,乙烷可与溴在光照下发生取代反应;
B.溴水或KMnO4溶液均与乙烯反应,与乙烷均不反应;
C.相同质量的乙烯和甲烷,含H的质量不同;
D.乙烯中含碳碳双键,乙烷中均为饱和键.
解答 解:A.乙烯与HBr发生加成反应生成溴乙烷,乙烷可与溴在光照下发生取代反应生成溴乙烷,故A正确;
B.溴水或KMnO4溶液均与乙烯反应,与乙烷均不反应,则溴水或KMnO4溶液都可以鉴别乙烯和乙烷,故B正确;
C.相同质量的乙烯和甲烷,含H的质量不同,由H原子守恒可知,完全燃烧后生成的水的质量不同,故C错误;
D.乙烯中含碳碳双键,乙烷中均为饱和键,则乙烯的化学性质比乙烷的化学性质活泼,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的组成、官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意性质的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.化学与科学、技术、社会、环境密切相关.下列有关说法中不正确的是( )
| A. | 屠呦呦女士利用乙醚萃取青蒿素获得了2015年度诺贝尔生理学或医学奖,为人类防治疟疾作出了重大贡献 | |
| B. | 光导纤维应避免在强碱性环境中使用 | |
| C. | 硅胶多孔、吸水能力强,常用作袋装食品的干燥 | |
| D. | 陶瓷、水泥、玻璃、大理石属于硅酸盐产品 |
16.用分液漏斗可以分离的一组混合物是( )
| A. | 溴苯和水 | B. | 甘油和水 | C. | 乙醇和乙二醇 | D. | 乙酸和乙醇 |
3.恒温恒容密闭容器中,能够表明反应A(s)+3B(g)?2C(g)+D(g)已达平衡的是( )
①混合气体的压强不变;
②混合气体的密度不变;
③B的物质的量浓度不变;
④容器内B、C、D三种气体的浓度比为3:2:1;
⑤混合气体的相对分子质量不变;
⑥消耗3molB的同时生成2molC.
①混合气体的压强不变;
②混合气体的密度不变;
③B的物质的量浓度不变;
④容器内B、C、D三种气体的浓度比为3:2:1;
⑤混合气体的相对分子质量不变;
⑥消耗3molB的同时生成2molC.
| A. | ①②③ | B. | ②③④ | C. | ②③⑤ | D. | ①③⑥ |
20.下列各组两种微粒间的关系与${\;}_{1}^{3}$H、${\;}_{1}^{2}$H之间关系相同的是( )
| A. | ${\;}_{8}^{18}$O,${\;}_{8}^{17}$O | B. | O2,O3 | C. | Fe3+,Fe2+ | D. | ${\;}_{6}^{12}$C,${\;}_{6}^{13}$C |
1.下列因果关系叙述正确的是( )
| A. | 浓HNO3的氧化性比稀HNO3,故有时在实验室看到的浓硝酸呈黄色 | |
| B. | Na的金属性比Mg强,故可用Na与MgCl2溶液反应制取Mg | |
| C. | Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中Fe也显+3价 | |
| D. | AlCl3易水解,故由AlCl3•6H2O制无水AlCl3应在HCl气流中加热 |


 ,在一定条件下Y与BrCl(一氯化溴,与卤素单质性质相似)按物质的量1:1发生加成反应,生成的产物可能有6种.
,在一定条件下Y与BrCl(一氯化溴,与卤素单质性质相似)按物质的量1:1发生加成反应,生成的产物可能有6种. .
.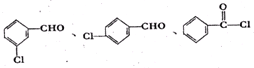 (不考虑立体异构).
(不考虑立体异构).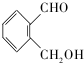 为有机原料制备化合物
为有机原料制备化合物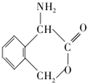 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).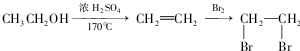 )
)