题目内容
如图所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲中盛放100mL6mol/L的盐酸,烧杯乙中盛放100mL冷水.现向烧杯甲的溶液中放入7.2g镁条,同时向烧杯乙中放人10g NH4Cl和20g氢氧化钡晶体,搅拌使之溶解.
(1)A瓶中气体颜色 ,理由是 ;
(2)B瓶中气体颜色 ,理由是 .
(1)A瓶中气体颜色

(2)B瓶中气体颜色
考点:化学平衡的影响因素
专题:
分析:根据温度对化学平衡的影响分析,Mg和盐酸反应使溶液温度升高,氯化铵和氢氧化钡反应使溶液温度降低,2NO2(g)?N2O4(g)△H<0,依据化学平衡移动原理分析,升温平衡向吸热方向进行,降温平衡向放热反应方向进行,二氧化氮是红棕色气体,四氧化二氮是无色气体.
解答:
解:(1)因Mg和盐酸反应使溶液温度升高,温度升高,平衡2NO2(g)?N2O4(g)△H<0向吸热方向移动,即逆反应方向移动,NO2浓度增大,颜色加深,
故答案为:变深;Mg与盐酸反应放热,所以A中气体温度升高.2NO2?N2O4(正反应为放热反应),平衡向左移动,NO2浓度增大,颜色加深;
(2)因氯化铵和氢氧化钡反应使溶液温度降低,使平衡2NO2(g)?N2O4(g)△H<0向放热热方向移动,即反应方向移动,NO2浓度减小,颜色变浅.
故答案为:变浅;NH4Cl与晶体氢氧化钡反应吸热,使B中气体温度降低,上述平衡向右移动,NO2浓度减小,颜色变浅.
故答案为:变深;Mg与盐酸反应放热,所以A中气体温度升高.2NO2?N2O4(正反应为放热反应),平衡向左移动,NO2浓度增大,颜色加深;
(2)因氯化铵和氢氧化钡反应使溶液温度降低,使平衡2NO2(g)?N2O4(g)△H<0向放热热方向移动,即反应方向移动,NO2浓度减小,颜色变浅.
故答案为:变浅;NH4Cl与晶体氢氧化钡反应吸热,使B中气体温度降低,上述平衡向右移动,NO2浓度减小,颜色变浅.
点评:本题结合实验考查了温度对化学平衡的影响,培养了学生灵活运用知识的能力.

练习册系列答案
相关题目
现有三组溶液,汽油和水的混合物;汽油和柴油的混合物;氯化钠和单质碘的水溶液,分离以上各混合物的正确方法依次是( )
| A、分液、蒸馏、萃取 |
| B、萃取、蒸馏、分液 |
| C、分液、萃取、蒸馏 |
| D、蒸馏、萃取、分液 |
实验是化学研究的基础.下列对实验现象的描述错误的是( )
 |  | 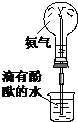 |  |
| ① | ② | ③ | ④ |
| A、实验①中溶液变黄色 |
| B、实验②试管中混合溶液变红色 |
| C、实验③中烧瓶内溶液变红色 |
| D、实验④中出现砖红色沉淀 |
如图所示的实验中,投入铝片后( )
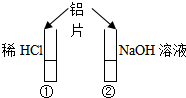

| A、①中产生气泡,②中不产生气泡片 |
| B、①和②中都不产生气泡稀HCl |
| C、①和②中都产生气泡,①中是H2,②中是O2 |
| D、①和②中都产生气泡,且都是H2①② |
相同质量的钠在下列情况下产生氢气最多的是( )
| A、投入到足量水中 |
| B、投入到足量盐酸中 |
| C、投入到足量CuSO4溶液中 |
| D、用刺有小孔的铝箔包好放入足量水中 |
钢铁在潮湿的空气中会被腐蚀,会发生的原电池反应.以下说法正确的是( )
| A、负极发生的反应为:Fe-3e-=Fe3+ |
| B、正极发生的反应为:2H2O+O2+4e-=4OH? |
| C、原电池是将电能转变为化学能的装置 |
| D、钢铁在水下部分比在空气与水交界处更容易腐蚀 |
照反应Br+H2?HBr+H的能量变化示意图,下列叙述正确的是( )
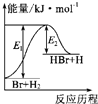

| A、该反应的△H=+(E1-E2)kJ?mol-1 |
| B、加入催化剂,该化学反应的反应热变大 |
| C、反应物的总能量高于生成物的总能量 |
| D、该反应为放热反应 |