题目内容
 某稀硫酸和硝酸的混合溶液200mL,分成两份.向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.
某稀硫酸和硝酸的混合溶液200mL,分成两份.向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.(1)第一份溶解铜粉的离子方程式
(2)第二份溶液中最终溶质为
(3)AB段的反应的化学方程式为
(4)原混合酸中HNO3的物质的量为
考点:有关混合物反应的计算
专题:
分析:由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,A点时,溶液中NO3-完全反应,此时消耗11.2g Fe,根据方程式计算每一份中HNO3的物质的量,进而原混合物中HNO3的物质的量;C点时反应完毕,共消耗Fe为22.4g,此时溶液中溶质为FeSO4,根据Fe原子守恒n(FeSO4)=n(Fe),根据硫酸根守恒n(H2SO4)=n(FeSO4),再根据c=
计算硫酸的物质的量浓度.
| n |
| V |
解答:
解:由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,
(1)第一份溶解铜粉的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
(2)由上述分析可知,第二份溶液中最终溶质为 FeSO4,BC段产生的气体是氢气,故答案为:FeSO4;H2;
(3)由上述分析可知,OA段产生的气体是NO,BC段产生的气体是H2,AB段的反应为:Fe+2Fe3+=3Fe2+,反应方程式为:Fe+Fe2(SO4)3=3FeSO4,
故答案为:Fe+Fe2(SO4)3=3FeSO4;
(4)A点时,溶液中NO3-完全反应,此时消耗11.2g Fe,其物质的量=
=0.2mol,由Fe+NO3-+4H+=Fe3++NO↑+2H2O,可知每一份溶液中n(HNO3)=n(NO3-)=n(Fe)=0.2mol,故原混合溶液中n(HNO3)=0.2mol×2=0.4mol;
C点时反应完毕,共消耗Fe为22.4g,其物质的量=
=0.4mol,此时溶液中溶质为FeSO4,根据Fe原子守恒n(FeSO4)=n(Fe)=0.4mol,根据硫酸根守恒n(H2SO4)=n(FeSO4)=0.4mol,故c=(H2SO4)=
=4mol/L,
故答案为:0.4;4.
(1)第一份溶解铜粉的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
(2)由上述分析可知,第二份溶液中最终溶质为 FeSO4,BC段产生的气体是氢气,故答案为:FeSO4;H2;
(3)由上述分析可知,OA段产生的气体是NO,BC段产生的气体是H2,AB段的反应为:Fe+2Fe3+=3Fe2+,反应方程式为:Fe+Fe2(SO4)3=3FeSO4,
故答案为:Fe+Fe2(SO4)3=3FeSO4;
(4)A点时,溶液中NO3-完全反应,此时消耗11.2g Fe,其物质的量=
| 11.2g |
| 56g/mol |
C点时反应完毕,共消耗Fe为22.4g,其物质的量=
| 22.4g |
| 56g/mol |
| 0.4mol |
| 0.1L |
故答案为:0.4;4.
点评:本题以图象为载体,考查有关金属和酸反应的计算题,难度中等,关键根据图象分析各段发生的反应,注意与铁的反应中硝酸全部起氧化剂作用

练习册系列答案
相关题目
一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是( )
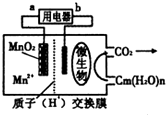

| A、电池工作时,电子由a流向b |
| B、微生物所在电极区放电时发生还原反应 |
| C、放电过程中,H+从正极区移向负极区 |
| D、正极反应式为:MnO2+4H++2e-═Mn2++2 H2O |
甲醇(CH3OH)是一种有毒物质,检测甲醇含量的测试仪工作原理示意图如下.下列说法正确的是( )

| A、该装置为电能转化为化学能的装置 |
| B、a电极发生的电极反应为CH3OH-6e-+H2O═CO2↑+6H+ |
| C、当电路中有1 mol e-转移时,正极区n(H+)增加1 mol |
| D、将酸性电解质溶液改为碱性电解质溶液该测试仪不可能产生电流 |
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、1mol[Cu(NH3)2]2+中含有σ键的数目为12NA |
| B、0.1mol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA |
| C、分子数目为0.1NA的N2和NH3混合气体,原子间含有的公共电子数目为0.3NA |
| D、用惰性电极电解CuSO4溶液一段时间后,若加入0.05mol的Cu2(OH)2CO3固体恰好能使溶液恢复到原来的浓度,则该电解过程中转移电子的数目为0.2NA |
下列说法正确的是( )
| A、石油裂解和油脂皂化都有高分子生成小分子的过程 |
| B、NOx、CO2、PM2.5颗粒都会导致酸雨 |
| C、工业上制备铝可用热还原的方法 |
| D、高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |

