题目内容
在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如下:则下列表述正确的是( )
| 四种物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 25 | 15 | 1 | 5 |
| 反应后质量(g) | 11 | 未测 | 1 | 22 |
| A、该反应是复分解反应 |
| B、丙一定是催化剂 |
| C、乙全部发生了反应 |
| D、甲与乙反应的质量比为14:3 |
考点:质量守恒定律
专题:守恒法
分析:利用质量守恒定律,反应前后各物质的质量总和相等,可计算出反应后未测的乙物质的质量;根据反应前后各物质的质量关系,对反应中各物质参与反应情况进行判断.
解答:
解:A.丙的质量在反应前后没有发生变化,根据质量守恒定律可知:该反应是化合反应,故A错误;
B.物质丙在反应前后质量不变,根据催化剂在反应前后质量和化学性质不变的特点,可推测该物质可能为反应的催化剂;但不能说一定是催化剂,故B错误;
C.根据质量守恒定律,未测物质乙的质量=(25+15+1+5)g-(11+1+22)g=12g,根据反应前后物质质量差可得知,反应中只有15g-12g=3g乙物质发生了反应,故C错误;:
D.根据质量守恒定律,甲与乙反应的质量比为(25-11):3=14:3,故D正确;
故选D.
B.物质丙在反应前后质量不变,根据催化剂在反应前后质量和化学性质不变的特点,可推测该物质可能为反应的催化剂;但不能说一定是催化剂,故B错误;
C.根据质量守恒定律,未测物质乙的质量=(25+15+1+5)g-(11+1+22)g=12g,根据反应前后物质质量差可得知,反应中只有15g-12g=3g乙物质发生了反应,故C错误;:
D.根据质量守恒定律,甲与乙反应的质量比为(25-11):3=14:3,故D正确;
故选D.
点评:对此类问题进行分析时,根据质量守恒定律计算出表中未测物质的质量,是需要首先解决的量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关实验室一般事故的预防和处理方法正确的是( )
| A、燃着的酒精灯打翻失火,应立即用水浇灭 |
| B、为了使过滤速率加快,可用玻棒在过滤器中轻轻搅拌,加速液体流动 |
| C、蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却 |
| D、皮肤上沾有少量浓硫酸,可立即用大量水冲洗 |
化学与生活密切相关.下列叙述错误的是( )
| A、氧化铁在涂料工业中用作红色防锈颜料 |
| B、铝制餐具不宜用来长时间存放酸性、碱性食物 |
| C、硅胶可用作袋装食品、瓶装药品等的干燥剂 |
| D、二氧化硫具有漂白性,可以用于食品增白 |
有Na2SO4和Al2(SO4)3的混合溶液,已知其中 c(Al3+)=0.4mol/L,c(SO42-)=0.7mol/L,则此溶液中c(Na+)为( )
| A、0.1mol/L |
| B、0.2mol/L |
| C、0.15mol/L |
| D、0.25mol/L |
下列化学用语表示正确的是( )
| A、质子数、中子数均为1的核素:1H |
| B、漂白粉的有效成分的化学式:CaClO |
C、Cl-的离子结构示意图: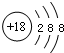 |
| D、碳酸钠的电离方程式:Na2CO3=2Na++CO32- |
下列有关化学用语的表示,正确的是( )
| A、乙烯的结构简式:CH2CH2 |
| B、醛基的结构简式:-COH |
C、丙烷分子的比例模型为: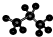 |
D、甲烷的电子式: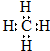 |
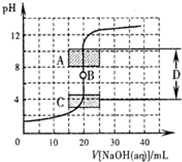 酸碱中和滴定是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法,其间溶液的pH变化是判断滴定终点的依据.
酸碱中和滴定是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法,其间溶液的pH变化是判断滴定终点的依据.