题目内容
19.钛合金被誉为二十一世纪的金属,具有广泛用途.下列是提炼金属属的反应之一:TiO2+2C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO 其中被氧化的元素是( )| A. | C | B. | Ti | C. | Cl | D. | Ti和C |
分析 TiO2+2C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO中,C元素的化合价升高,Cl元素的化合价降低,以此来解答.
解答 解:TiO2+2C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO中,C元素的化合价升高,C失去电子被氧化,
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念及分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
9.下列实验操作不能达到实验目的是( )
| A. | 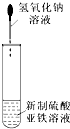 可以制备Fe(OH)2并可以较长时间观察到Fe(OH)2的颜色 | |
| B. | 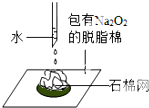 可以证明过氧化钠与水反应是放热反应 | |
| C. | 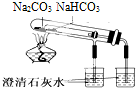 可以证明碳酸钠热稳定性比碳酸氢钠好 | |
| D. | 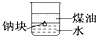 可以证明密度:ρ(煤油)<ρ(钠)<ρ(水) |
10.下列图示的四种实验操作名称从左到右依次是( )
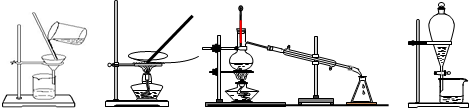

| A. | 过滤、蒸发、蒸馏、萃取分液 | B. | 过滤、蒸馏、蒸发、萃取分液 | ||
| C. | 蒸发、蒸馏、过滤、萃取分液 | D. | 萃取分液、蒸馏、蒸发、过滤 |
7.下列离子方程式正确的是( )
| A. | 硫化钠水解:S2-+2H2O?H2S+2OH- | |
| B. | 硫氢化钠的水解:HS-+H2O?H3O++S2- | |
| C. | 不断加热煮沸氯化铁溶液:Fe3++3H2O?Fe(OH)3+3H+ | |
| D. | NH4Cl水解:NH4++H2O?NH3•H2O+H+ |
11.下列物质间的转化,通过一步反应不能完成的是( )
| A. | FeCl3→FeCl2 | B. | NO2→HNO3 | C. | Al2O3→NaAlO2 | D. | SiO2→H2SiO3 |
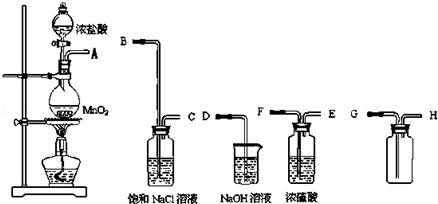
9.下列装置所示的实验中,能达到实验目的是( )
| A. | 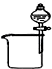 分离碘和酒精 | B. | 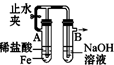 较长时间观察Fe (OH)2白色沉淀 | ||
| C. | 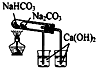 验证NaHCO3和Na2CO3的热稳定性 | D. |  除去Cl2中HCl |
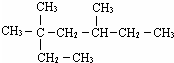 3,3,5-三甲基庚烷
3,3,5-三甲基庚烷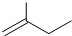 C5H10.
C5H10.