题目内容
18.下列装置工作-段时间后.各池出现了不同现象.下列有关说法不正确的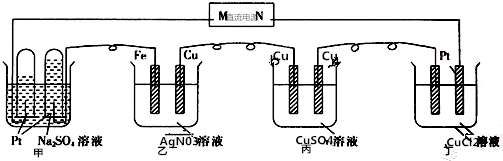
| A. | N为直流电源的正极 | |
| B. | 乙池的总反应为4AgN03+2H20═4Ag+4HNO3+O2↑ | |
| C. | 丙池的反应符合电解精炼铜原理 | |
| D. | 要使丁池电解质溶液复原,需加适量的CuCl2 |
分析 甲池中的两个电极上产生无色气体氢气和氧气,氢气体积是氧气的2倍,所以左边电极上产生的是氢气,该电极上是阴极,另一电极是阳极,所以M是负极,N是正极,乙装置中Fe是阳极,Cu是阴极,根据电解池的工作原理以及电解质复原的方法来回答.
解答 解:A、甲池中的两个电极上产生无色气体氢气和氧气,氢气体积是氧气的2倍,所以左边电极上产生的是氢气,该电极上是阴极,另一电极是阳极,所以M是负极,N是正极,故A正确;
B、乙装置中Fe是阳极,在阳极上是金属铁是电子的,Cu是阴极,乙池的总反应为2AgN03+Fe═2Ag+Fe(NO3)2,故B错误;
C、电解精炼铜原理:粗铜是阳极,精通是阴极,电解质可以选择硫酸铜,该装置符合,故C正确;
D、丁池的电解实质是电解氯化铜本身,要使丁池电解质溶液复原,需加适量的CuCl2,故D正确.
故选B.
点评 本题考查学生电解池的工作原理以及应用知识,注意知识的归纳和梳理是解题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.几种短周期元素的原子半径和主要化合价见下表,下列说法中正确的是( )
| 元素代号 | 原子半径/nm | 主要化合价 |
| X | 0.160 | +2 |
| Y | 0.143 | +3 |
| Z | 0.102 | +6、-2 |
| L | 0.099 | +7、-1 |
| M | 0.077 | +4、-4 |
| Q | 0.074 | -2 |
| A. | Z的氢化物的稳定性强于L的氢化物的稳定性 | |
| B. | Y与Q形成的化合物不能跟氢氧化钠溶液反应 | |
| C. | 等物质的量的X、Y的单质与足量的盐酸反应,生成的H2一样多 | |
| D. | 在化学反应中,M原子与其他原子易形成共价键而不易形成离子键 |
9.用下列实验装置进行相应实验,能达到实验目的是( )
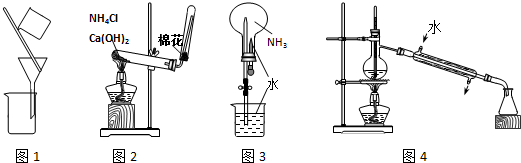

| A. | 用图1装置分离乙醇和乙酸 | B. | 用图2装置制取氨气 | ||
| C. | 用图3装置进行氨气的喷泉实验 | D. | 用图4装置进行石油的分馏实验 |
6.判断下列元素中不属于主族元素的是( )
| A. | 钡 | B. | 铅 | C. | 碘 | D. | 铁 |
13.标况下,某混合气体由两种气态烃组成,2.24L该混合气体完全燃烧后,得到4.48L二氧化碳和3.6克水,则这两种气体可能是( )
| A. | CH4和 C3H8 | B. | CH4和C3H4 | C. | C2H2和C3H4 | D. | C2H4和C2H6 |
3.下列化合物中既有离子键又有共价键的是( )
| A. | MgCl2 | B. | NaOH | C. | HBr | D. | N2 |
10.下列有关叙述中正确的是( )
| A. | 溶液中大量共存:Na+、Ba2+、Cl-、CO32- | |
| B. | 无色溶液中能大量共存:NH4+、Fe3+、SO42-、CI- | |
| C. | 氢氧化铁跟硫酸反应的离子方程式是:3H++Fe(OH)3═Fe3++3H2O | |
| D. | 碳酸氢钠溶液跟氢氧化钠反应的离子方程式是:HCO3-+OH-═H2O+CO2↑ |
8.实验室保存下列物质的方法中,不正确的是( )
| A. | 少量金属钠保存在煤油里 | |
| B. | 浓硫酸存放在广口试剂瓶中 | |
| C. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| D. | 氯水应装在棕色细口瓶中密封避光保存 |