题目内容
 乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:已知:①氯化钙可与乙醇形成CaCl2?6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
| 浓硫酸 |
| 140℃ |
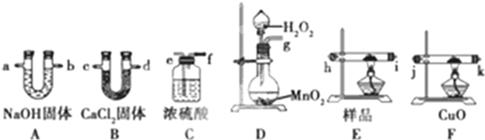
I.制备过程:装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液.
(1)写出乙酸与乙醇发生酯化反应的化学方程式
(2)浓硫酸对该乙酸乙酯合成反应的影响是:
(3)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是
A.25mL B.50mL C.250mL D.500mL
(4)设计简单实验证明饱和碳酸钠溶液是否起到了吸收乙酸的作用:
(5)实验过程中发现两层之间出现了白色固体,请用化学方程式表示形成原因:
Ⅱ.提纯方法
①将D中混合液转入分液漏斗进行分液.
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤.有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物.
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯.
(6)第①步分液时,选用的两种玻璃仪器的名称分别是
(7)第②步中用饱和食盐水、饱和氯化钙溶液、最后用水洗涤,分别主要洗去粗产品中的
考点:乙酸乙酯的制取
专题:实验设计题
分析:(1)根据酯化反应原理,羧酸脱去羟基醇脱氢写出化学方程式;
(2)乙酸与乙醇在浓硫酸作催化剂、加热的条件下发生酯化反应生成乙酸乙酯,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(3)烧瓶中液体的体积不超过烧瓶容积的
且不少于
;
(4)碳酸钠水解显碱性,若碱性减弱,证明碳酸钠和乙酸反应;
(5)碳酸钠和乙酸反应生成碳酸氢钠和乙酸钠,碳酸氢钠溶解度小,生成碳酸氢钠较多会析出沉淀;
(6)根据分液操作用到的仪器回答;
(7)碳酸钠在饱和食盐水中易溶,乙酸乙酯溶解度减小;饱和氯化钙能与乙醇发生反应生成CaCl2?6C2H5OH;水洗涤除掉吸附的氯化钙.
(2)乙酸与乙醇在浓硫酸作催化剂、加热的条件下发生酯化反应生成乙酸乙酯,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(3)烧瓶中液体的体积不超过烧瓶容积的
| 2 |
| 3 |
| 1 |
| 3 |
(4)碳酸钠水解显碱性,若碱性减弱,证明碳酸钠和乙酸反应;
(5)碳酸钠和乙酸反应生成碳酸氢钠和乙酸钠,碳酸氢钠溶解度小,生成碳酸氢钠较多会析出沉淀;
(6)根据分液操作用到的仪器回答;
(7)碳酸钠在饱和食盐水中易溶,乙酸乙酯溶解度减小;饱和氯化钙能与乙醇发生反应生成CaCl2?6C2H5OH;水洗涤除掉吸附的氯化钙.
解答:
解:(1)由于酯化反应中,羧酸脱去的是羟基,反应方程式为CH3COOH+C2H5OH
CH3COOC2H5+H2O,故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O;
(2)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,故浓硫酸的作用为:催化剂、吸水剂,
故答案为:浓硫酸在反应中起催化剂作用,可加快反应速率;浓硫酸有吸水性,有利于反应向生成酯的方向移动,提高产率;
(3)烧瓶内的液体体积约为3ml+9.5ml+6ml=18.5mol,烧瓶中液体的体积不超过烧瓶容积的
且不少于
,因此50ml符合,
故答案为:B;
(4)碳酸钠水解显碱性,若碱性减弱,证明碳酸钠和乙酸反应;
故答案为:向饱和碳酸钠溶液中滴入几滴酚酞,溶液红色逐渐变浅即证明饱和碳酸钠溶液起到了吸收乙酸的作用;
(5)碳酸钠和乙酸反应生成碳酸氢钠和乙酸钠,反应方程式为:Na2CO3+CH3COOH=NaHCO3↓+CH3COONa,碳酸氢钠溶解度小,生成碳酸氢钠较多会析出沉淀;
故答案为:Na2CO3+CH3COOH=NaHCO3↓+CH3COONa;
(6)分液操作中用到的主要仪器是分液漏斗,烧杯作为盛放分层液体的容器,
故答案为:分液漏斗;烧杯;
(7)碳酸钠在饱和食盐水中易溶,乙酸乙酯溶解度减小,故选用饱和食盐水除去乙酸乙酯中的碳酸钠杂质;饱和氯化钙能与乙醇发生反应生成CaCl2?6C2H5OH,因此用饱和氯化钙溶液除掉乙醇;水洗涤除掉吸附的氯化钙,
故答案为:碳酸钠;乙醇;氯化钙.
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
(2)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,故浓硫酸的作用为:催化剂、吸水剂,
故答案为:浓硫酸在反应中起催化剂作用,可加快反应速率;浓硫酸有吸水性,有利于反应向生成酯的方向移动,提高产率;
(3)烧瓶内的液体体积约为3ml+9.5ml+6ml=18.5mol,烧瓶中液体的体积不超过烧瓶容积的
| 2 |
| 3 |
| 1 |
| 3 |
故答案为:B;
(4)碳酸钠水解显碱性,若碱性减弱,证明碳酸钠和乙酸反应;
故答案为:向饱和碳酸钠溶液中滴入几滴酚酞,溶液红色逐渐变浅即证明饱和碳酸钠溶液起到了吸收乙酸的作用;
(5)碳酸钠和乙酸反应生成碳酸氢钠和乙酸钠,反应方程式为:Na2CO3+CH3COOH=NaHCO3↓+CH3COONa,碳酸氢钠溶解度小,生成碳酸氢钠较多会析出沉淀;
故答案为:Na2CO3+CH3COOH=NaHCO3↓+CH3COONa;
(6)分液操作中用到的主要仪器是分液漏斗,烧杯作为盛放分层液体的容器,
故答案为:分液漏斗;烧杯;
(7)碳酸钠在饱和食盐水中易溶,乙酸乙酯溶解度减小,故选用饱和食盐水除去乙酸乙酯中的碳酸钠杂质;饱和氯化钙能与乙醇发生反应生成CaCl2?6C2H5OH,因此用饱和氯化钙溶液除掉乙醇;水洗涤除掉吸附的氯化钙,
故答案为:碳酸钠;乙醇;氯化钙.
点评:本题考查了乙酸乙酯的制备,题目难度中等,该实验要关注制备的细节如反应条件,催化剂的使用及其产物的除杂提纯等问题.

练习册系列答案
相关题目
两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n.下列说法错误的是( )
| A、若a=b=3,8>m>n>b,则元素非金属性:X>Y |
| B、若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y<X |
| C、若Y的气态氢化物化学式为YHn,且b<4,则该氢化物易溶于水 |
| D、若a<b=3,m=n=7,已知原子半径大小:Y>N(氮原子)>X,则NX3、NY3与水反应生成不同的含氮化合物 |
下列离子方程式正确的是( )
| A、将少量石灰水滴入碳酸氢钠溶液中 HCO3-+Ca2++OH-═CaCO3↓+H2O | ||||
B、碳酸氢铵与足量氢氧化钠两种浓溶液混合加热 NH4++OH-
| ||||
| C、用惰性电极电解氯化钠溶液 2H2O+2Cl-═Cl2↑+H2↑+2OH- | ||||
| D、亚硝酸钠水溶液显碱性 NO2-+H2O?HNO2+OH- |
取一定质量含Cu、Cu2O、CuO的固体混合物,将其分成两等份并进行下列转化,
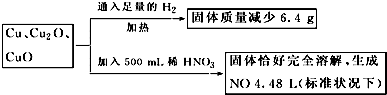
则转化过程中所加稀HNO3的物质的量浓度为( )

则转化过程中所加稀HNO3的物质的量浓度为( )
| A、4.4 mol?L-1 |
| B、3.6 mol?L-1 |
| C、4.0 mol?L-1 |
| D、3.2 mol?L-1 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1molCl2常温下与过量NaOH溶液反应转移电子总数为0.1NA |
| B、25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
| C、0.25molNa2O2中含有的阴离子数为0.5NA |
| D、18gD2O(重水)完全电解,转移的电子数为NA |