题目内容
(1)18O2-离子结构示意图 ,质量相等的O3和O2中,原子个数之比为 ;
(2)某硫原子的质量是a g,12C原子的质量是b g,若NA只表示阿伏加德罗常数的数值,则该硫原子的相对原子质量为 ,m g该硫原子的物质的量为 mol;
(3)19g 某二价金属的氯化物ACl2 中含有0.4molCl-,ACl2的摩尔质量 .
(2)某硫原子的质量是a g,12C原子的质量是b g,若NA只表示阿伏加德罗常数的数值,则该硫原子的相对原子质量为
(3)19g 某二价金属的氯化物ACl2 中含有0.4molCl-,ACl2的摩尔质量
考点:物质的量的相关计算
专题:计算题
分析:(1)18O2-离子核外有10个电子,有2个电子层,各层电子数为2、8;O3和O2都由同种氧原子构成,二者质量相等,所含氧原子数目相同;
(2)以一个12C原子质量的
为标准,其他原子的质量跟它相比较所得到的比值,即为这种原子的相对原子质量;摩尔质量以g/mol作单位,数值上等于该物质的相对分子质量或相对原子质量;根据n=
计算S原子物质的量;
(3)根据Cl-离子物质的量计算n(ACl2),再根据M=
计算ACl2的摩尔质量.
(2)以一个12C原子质量的
| 1 |
| 12 |
| m |
| M |
(3)根据Cl-离子物质的量计算n(ACl2),再根据M=
| m |
| M |
解答:
解:(1)18O原子核外有8个电子,有2个电子层,各层电子数为2、6,原子结构示意图为: ;O3和O2都由同种氧原子构成,二者质量相等,含有氧原子数目相等,即含有氧原子数目之比为1:1,
;O3和O2都由同种氧原子构成,二者质量相等,含有氧原子数目相等,即含有氧原子数目之比为1:1,
故答案为: ;1:1;
;1:1;
(2)一个12C的质量是bg,一个S原子的质量是ag,则该S原子的相对原子质量为
=
;1mol某S原子的质量为aNAg,S原子的摩尔质量和其相对原子质量数值相等,故S原子的相对原子质量为aNA,m g该硫原子的物质的量为
=
mol或为
=
mol,
故答案为:
或aNA;
或
;
(3)19g某二价金属的氯化物ACl2中含有0.4molCl-,则n(ACl2)=
=0.2mol,故ACl2的摩尔质量=
=95g/mol,
故答案为:95g/mol.
 ;O3和O2都由同种氧原子构成,二者质量相等,含有氧原子数目相等,即含有氧原子数目之比为1:1,
;O3和O2都由同种氧原子构成,二者质量相等,含有氧原子数目相等,即含有氧原子数目之比为1:1,故答案为:
 ;1:1;
;1:1;(2)一个12C的质量是bg,一个S原子的质量是ag,则该S原子的相对原子质量为
| ag | ||
|
| 12a |
| b |
| mg | ||
|
| bm |
| 12a |
| mg |
| aNAg/mol |
| m |
| aNA |
故答案为:
| 12a |
| b |
| bm |
| 12a |
| m |
| aNA |
(3)19g某二价金属的氯化物ACl2中含有0.4molCl-,则n(ACl2)=
| 0.4mol |
| 2 |
| 19g |
| 0.2mol |
故答案为:95g/mol.
点评:本题考查化学计算,涉及相对原子质量计算、物质的量计算、化学式的有关计算等,难度中等,(2)中注意对相对原子质量的理解.

练习册系列答案
相关题目
已知25℃、101kPa下,含1mol碳原子的石墨完全燃烧生成CO2放出热量393.51kJ;含1mol碳原子的金刚石完全燃烧生成CO2放出395.41kJ的热量.据此判断,下列说法正确的是( )
| A、由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低 |
| B、由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高 |
| C、由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低 |
| D、由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高 |
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水.当生成1mol硝酸锌时,参加反应硝酸的物质的量为( )
| A、2mol |
| B、3 mol |
| C、2.25mol |
| D、2.5mol |

 如图中的①、②、③、④分别是几种常见漏斗的上部,A、B、C、D分别是实际操作时,各漏斗的下部插入容器的示意图.请根据实际使用操作时上述漏斗的使用范围和它们形状,指出①、②、③、④分别与A、B、C、D中的哪一种或几种相匹配?
如图中的①、②、③、④分别是几种常见漏斗的上部,A、B、C、D分别是实际操作时,各漏斗的下部插入容器的示意图.请根据实际使用操作时上述漏斗的使用范围和它们形状,指出①、②、③、④分别与A、B、C、D中的哪一种或几种相匹配?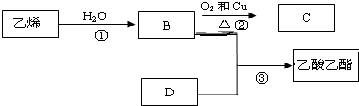 已知各物质能发生以下转化,根据框图回答:
已知各物质能发生以下转化,根据框图回答: