题目内容
16.A、B、C、D四种短周期主族元素的原子序数依次减小;在短周期的主族元素中D的原子半径最大;C原子最外层电子数与电子层数相等;B元素的主要化合价:最高正价+最低负价=4.下列说法正确的是( )| A. | A、C、D最高价氧化物对应的水化物两两之间能发生反应 | |
| B. | D和A能形成原子个数比为2:1型的离子化合物 | |
| C. | 最高价氧化物对应的水化物的酸性:B>A | |
| D. | C的氧化物是碱性氧化物 |
分析 A、B、C、D四种短周期主族元素的原子序数依次减小,D在短周期主族元素中原子半径最大,则D为Na;B元素的主要化合价:最高正价+最低负价=4,处于ⅥA族,故B为S元素;C原子序数大于Na、小于S,故C处于第三周期,而C原子最外层电子数与电子层数相等,故C为Al;A的原子序数大于硫,故A为Cl,据此解答.
解答 解:A、B、C、D四种短周期主族元素的原子序数依次减小,D在短周期主族元素中原子半径最大,则D为Na;B元素的主要化合价:最高正价+最低负价=4,处于ⅥA族,故B为S元素;C原子序数大于Na、小于S,故C处于第三周期,而C原子最外层电子数与电子层数相等,故C为Al;A的原子序数大于硫,故A为Cl.
A.A为Cl元素,C为Al元素,D为Na元素,三种元素氧化物对应水化物分别为NaOH、Al(OH)3、HClO4,两两之间能够反应,故A正确;
B.D与A能形成NaCl,能形成原子个数比为1:1型的离子化合物,故B错误;
C.由于非金属性A(Cl)>B(S),故最高价氧化物对应水化物的酸性:高氯酸>硫酸,故C错误;
D.C为Al元素,铝的氧化物为两性氧化物,故D错误,
故选A.
点评 本题考查位置结构性质关系应用,根据原子结构和性质来推断元素是解题关键,题目难度中等,注意把握元素化合物的性质和元素周期律,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
6.甲、乙两种非金属,①甲比乙容易与H2化合;②甲的单质能与乙的阴离子发生氧化还原反应;③甲的最高价氧化物的水化物酸性比乙的最高价氧化物的水化物的酸性强;④与某金属反应时甲原子得电子数比乙的多;⑤甲的单质熔沸点比乙的低.能说明甲比乙的非金属性强的是( )
| A. | 只有④ | B. | 只有⑤ | C. | ①②③ | D. | 全部 |
7.下列实验现象不能实验预期的目的是( )
| A. | 用食醋,石灰水来验证蛋壳的成分是碳酸盐 | |
| B. | 用银氨溶液鉴别乙醇和乙醛 | |
| C. | 用酸性高锰酸钾验证苯中是否含有碳碳双键 | |
| D. | 用溴水鉴别乙烯和乙炔 |
4.乙醇和甘油、苯酚的共同点是( )
| A. | 都能和氢氧化钠发生中和反应 | B. | 都能与金属钠反应产生氢气 | ||
| C. | 都能与FeCl3溶液反应显紫色 | D. | 都属于酚类化合物 |
11.表是元素周期表的一部分,请参照元素
(1)①~⑨中金属性最强的元素是(填元素符号)Na,非金属性最强的元素是(填元素符号)F.
(2)④、⑤、⑦的原子半径由大到小的顺序为(填元素符号)Na>Al>O.
(3)②、③的最高价氧化物的水化物的酸性强弱顺序为(填化学式)HNO3>H2CO3.
(4)由①、④元素按原子个数比2:1组成的化合物的电子式为 .
.
(5)由②和④组成的化合物与⑥单质反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(6)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑨ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)④、⑤、⑦的原子半径由大到小的顺序为(填元素符号)Na>Al>O.
(3)②、③的最高价氧化物的水化物的酸性强弱顺序为(填化学式)HNO3>H2CO3.
(4)由①、④元素按原子个数比2:1组成的化合物的电子式为
 .
.(5)由②和④组成的化合物与⑥单质反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(6)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
1.已知12g石墨完全转化为金刚石时,要吸收EkJ的能量,下列说法正确的是( )
| A. | 金刚石与石墨互为同位素 | |
| B. | 石墨不如金刚石稳定 | |
| C. | 金刚石比石墨能量低 | |
| D. | 等质量的石墨与金刚石完全燃烧,金刚石放出的能量多 |
8.化学反应中一定伴随着能量的变化,下列有关能量的说法正确的是( )
| A. | 等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 | |
| B. | 由C(石墨)?C(金刚石)△H=+1.9kJ/mol可知,金刚石比石墨稳定 | |
| C. | 根据热化学方程式:S(s)+O2(g)?SO2(g)△H=-297.23kJ/mol,可推知1 mol SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和 | |
| D. | 根据稀溶液中反应:H+(aq)+OH-(aq)?H2O(l)△H=-57.3kJ/mol;若将含0.5 mol H2SO4的浓硫酸与含l mol NaOH的稀溶液混合时,放出的热量大于57.3 kJ |
5.用一定量的SO2和O2在容积固定的2L密闭容器内发生反应:2SO2+O2?2SO3,如果v(SO2)=0.05mol/(L•min),则2min后SO3的物质的量为( )
| A. | 0.2 mol | B. | 0.1 mol | C. | 0.2 mol/L | D. | 0.1 mol/L |
1.有机物的种类繁多,但其命名是有规则的.下列有机物命名正确的是( )
| A. | 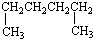 1,4-二甲基丁烷 1,4-二甲基丁烷 | B. | 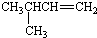 3-甲基丁烯 3-甲基丁烯 | ||
| C. | 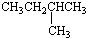 2-甲基丁烷 2-甲基丁烷 | D. | CH2Cl-CH2Cl 二氯乙烷 |