题目内容
19.已知:①CH4(g)+4N02(g)═4NO(g)+2H2O(g)△H1=-574KJ•mol-1
②CH4(g)+4N0(g)═2N2(g)+CO2+2H2O(g)△H2=-1160KJ•mol-1
则CH4催化还原NOX的相关说法正确的是( )
| A. | 由①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(1)的△H大于△H1 | |
| B. | 等物质的量的甲烷分别发生①②反应至完全,转移的电子数不同 | |
| C. | 若用0.2 mol CH4发生上述反应还原足量的NO2至N2,放出的热量为173.4 kJ | |
| D. | 若用标准状况下4.48 LCH4还原足量的NO2至N2,整个过程中转移的电子的物质的量为16 mol |
分析 A.由气态水变为液态,放出热量;
B.根据C元素的化合价变化来计算转移的电子;
C.反应 $\frac{①+②}{2}$可知CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g),分析物质的量与反应热的数值关系;
D.反应 $\frac{①+②}{2}$可知CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g),1molCH4反应转移8mol电子.
解答 解:A.由CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1,水由气态变为液态,放出热量,则CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)△H=-Q,Q>574kJ•mol-1,焓变均为负数,则△H小于△H1,故A错误;
B.两个反应中,C元素的化合价均由-4价升高到+4价,则等物质的量的甲烷分别参加反应①、②,反应转移的电子数相同,故B错误;
C.反应 $\frac{①+②}{2}$可知CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g),CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g)△H=-867kJ/mol,标准状况下物质的量为0.2molCH4,则放出的热量为0.2mol×867kJ=173.4kJ,故C正确;
D.CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g),1molCH4反应转移8mol电子,则用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为0.2mol×8=1.6mol,故D错误;
故选C.
点评 本题考查氧化还原反应及焓变,为高频考点,把握盖斯定律的应用及反应中物质的量与反应能量变化的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的燃烧热为241.8kJ•mol-1 | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知2C(s)+2O2(g)═2CO2 (g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 | |
| D. | 已知Ni(CO)4(s)═Ni(s)+4CO(g)△H=Q kJ•mol-1,则Ni(s)+4CO(g)═Ni(CO)4(s)△H=-QkJ•mol-1 |
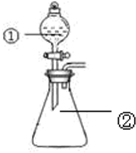 用如图所示装置进行下列实验:将①中溶液滴入②锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②锥形瓶中,预测的现象与实际相符的是( ) | 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D. | SO2饱和溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 金属氧化物 氧化铁 FeO | |
| B. | 非金属氧化物 二氧化硫 SO2 | |
| C. | 碱性氧化物 过氧化钠 Na2O2 | |
| D. | 碱 纯碱 Na2CO3 |
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 离子的还原性:S2->Cl->Br->I- | |
| C. | 酸性:H2SO4>H3PO4>H2CO3>HClO | |
| D. | 金属性:Be<Mg<Ca<K |
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温条件下一定能自发进行 | |
| C. | 反应物和生成物所具有的总焓决定了反应是放热还是吸热 | |
| D. | 放热反应在任何条件下也能发生反应 |