题目内容
17.现有镁铝铜合金1.22g,加入过量的盐酸中,在标准状况下放出氢气1.12L,反应后过滤得沉淀0.2g.若将此合金放入过量的烧碱溶液中,反应后,在标准状况下,产生氢气的体积约为多少?分析 加入过量盐酸发生反应:Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑,反应后过滤的沉淀0.2g为Cu的质量,根据金属总质量、生成氢气的物质的量列式计算出各计算的物质的量,将此合金放入过量的烧碱溶液中,发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据铝的物质的量计算出生成氢气在标况下的体积.
解答 解:由题意可知m(Cu)=0.2 g,故合金中Mg、Al总质量为1.22g-0.2g=1.02g,
设Mg为xmol,Al为ymol,则:
Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑
xmol xmol ymol 1.5mol
可得关系式:24 g/mol×xmol+27 g/mol×ymol=1.02 g
x mol+1.5y mol=$\frac{1.12L}{22.4L/mol}$=0.05mol
联立方程解得:x=y=0.02
将此合金放入过量的烧碱溶液中,只发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,则生成氢气为0.02mol×$\frac{3}{2}$×22.4L/mol=0.672L,
答:将此合金放入过量的烧碱溶液中,反应后在标准状况下产生氢气的体积约为0.672L.
点评 本题考查混合物的计算,明确发生的反应即可解答,也可利用电子转移守恒计算,试题有利于培养学生的化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8g O2的体积为5.6L | |
| B. | 标准状况下,22.4 L H2O所含的分子数为NA | |
| C. | 标准状况下,50mL 0.2mol•L-1的盐酸中含有分子数为0.01NA | |
| D. | 常温常压下,10g氖气含有的原子数为0.5NA个 |
9.下列物质的分子中,共用电子对数目最多的是( )
| A. | N2 | B. | NH3 | C. | CO2 | D. | CH4 |
5.下列事实中,不能用勒夏特列原理解释的是( )
| A. | 冰镇的啤酒打开后泛起泡沫 | |
| B. | 500℃左右比室温更有利于合成氨的反应(△H<0) | |
| C. | 红棕色的NO2加压后颜色先变深再变浅(2 NO2?N2O4(无色)) | |
| D. | 光照新制的氯水时,溶液的pH逐渐减小 |
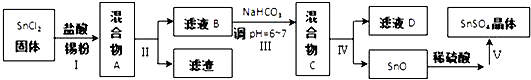
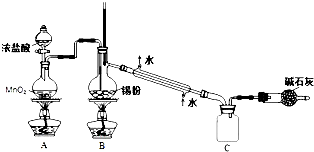
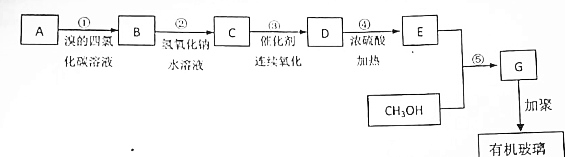
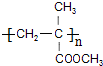 .
.