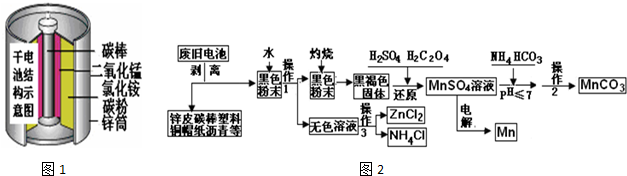
题目内容
5.现有A、B、C、D、E五种元素,它们的核电荷数依次增大,且均小于20.其中只有C、E是金属元素,A、E最外层上都只有一个电子,B、D元素原子最外层电子数相同,且B元素L层电子数是K层的3倍,C元素最外层电子数是D元素最外层电子数的一半.请回答:(1)它们各是什么元素?(用元素名称回答)A氢 C氯 D硫.
(2)写出B元素离子的电子式
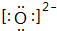 .
.(3)写出E元素原子的结构示意图
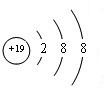 .
.(4)写出与E元素的离子具有相同电子层排布的两种微粒的符号S2-、Ca2+.
(5)A、B两元素间可以形成的化合物有H-O-H、H-O-O-H(用结构式回答)
分析 A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,B和D元素原子的最外层电子数相同,二者处于同主族,且B原子L层电子数是K层电子数的3倍,则B原子L层电子数为6,故B为氧元素、D为硫元素;只有C、E是金属元素,A和E原子的最外层电子都只有一个,二者处于ⅠA族,结合原子序数可知,E为K元素、A为氢元素;C元素原子的最外层电子数是D元素原子最外层电子数的一半,最外层电子数为3,结合原子序数可知C为Al,据此解答.
解答 解:A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,B和D元素原子的最外层电子数相同,二者处于同主族,且B原子L层电子数是K层电子数的3倍,则B原子L层电子数为6,故B为氧元素、D为硫元素;只有C、E是金属元素,A和E原子的最外层电子都只有一个,二者处于ⅠA族,结合原子序数可知,E为K元素、A为氢元素;C元素原子的最外层电子数是D元素原子最外层电子数的一半,最外层电子数为3,结合原子序数可知C为Al.
(1)由上述分析可知,A为氢元素、C为铝、D为硫元素,故答案为:氢;铝;硫;
(2)B元素离子为O2-,电子式为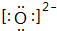 ,故答案为:
,故答案为: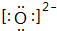 ;
;
(3)E为K元素素,原子的结构示意图为 ,故答案为:
,故答案为: ;
;
(4)E元素的离子为K+,具有相同电子层排布的两种微粒的符号:S2-、Ca2+等,故答案为:S2-;Ca2+;
(5)A、B两元素间可以形成的化合物有H2O、H2O2,它们的结构式分别为:H-O-H、H-O-O-H,故答案为:H-O-H;H-O-O-H.
点评 本题考查结构性质位置关系,推断元素是解答的关键,题目难度不大,旨在考查学生对基础知识的掌握.

练习册系列答案
相关题目
15. 海水中主要离子的含量如下:
海水中主要离子的含量如下:
(1)常温下,海水的pH在7.5~8.6之间,其原因是(用离子方程式表示)HCO3-+H2O?H2CO3+OH-.
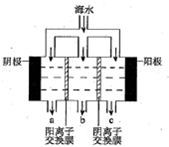
(2)电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.阴极上产生氢气,阴极附近还产生少量白色沉淀,其成分有Mg(OH)2和CaCO3,生成CaCO3的离子方程式是Ca2++OH-+HCO3-=CaCO3↓+H2O.
(3)用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:
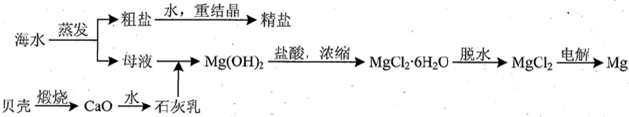
①在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发…洗涤等步骤;有关其中“蒸发”步骤的叙述正确的是bd.
a.蒸发的目的是得到热饱和溶液
b.蒸发的目的是析出晶体
c.应用余热蒸干溶液
d.应蒸发至有较多晶体析出时为止
②由MgCl2溶液得到MgCl2•6H2O晶体时,也需要蒸发,蒸发的目的是得到热饱和溶液,判断溶液已饱和的现象是溶液表面形成晶膜.
(4)25℃时,饱和Mg(OH)2溶液的浓度为5×10-4 mol/L.
①饱和Mg(OH)2溶液中滴加酚酞,现象是溶液变红.
②某学习小组测海水中Mg2+含量(mg/L)的方法是:取一定体积的海水,加入足量盐酸,再加入足量NaOH,将Mg2+转为Mg(OH)2.25℃,该方法测得的Mg2+含量与表中1272mg/L的“真值”比,相对误差约为-5.6%[保留2位小数,海水中饱和Mg(OH)2溶液的密度都以l g/cm3计].
 海水中主要离子的含量如下:
海水中主要离子的含量如下:| 成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
(2)电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.阴极上产生氢气,阴极附近还产生少量白色沉淀,其成分有Mg(OH)2和CaCO3,生成CaCO3的离子方程式是Ca2++OH-+HCO3-=CaCO3↓+H2O.
(3)用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:

①在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发…洗涤等步骤;有关其中“蒸发”步骤的叙述正确的是bd.
a.蒸发的目的是得到热饱和溶液
b.蒸发的目的是析出晶体
c.应用余热蒸干溶液
d.应蒸发至有较多晶体析出时为止
②由MgCl2溶液得到MgCl2•6H2O晶体时,也需要蒸发,蒸发的目的是得到热饱和溶液,判断溶液已饱和的现象是溶液表面形成晶膜.
(4)25℃时,饱和Mg(OH)2溶液的浓度为5×10-4 mol/L.
①饱和Mg(OH)2溶液中滴加酚酞,现象是溶液变红.
②某学习小组测海水中Mg2+含量(mg/L)的方法是:取一定体积的海水,加入足量盐酸,再加入足量NaOH,将Mg2+转为Mg(OH)2.25℃,该方法测得的Mg2+含量与表中1272mg/L的“真值”比,相对误差约为-5.6%[保留2位小数,海水中饱和Mg(OH)2溶液的密度都以l g/cm3计].
20.下列叙述中,肯定能说明金属甲比金属乙金属性强的是( )
| A. | 甲原子最外层电子数比乙原子最外层电子数少 | |
| B. | 甲原子电子层数比乙原子电子层数多 | |
| C. | 1mol甲从酸中置换生成的氢气比1mol乙从酸中置换生成的氢气多 | |
| D. | 常温下,甲能与水反应生成氢气,而乙不能 |
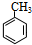
15.下列对有机物结构或性质的描述中错误的是( )
| A. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 | |
| B. | 乙烷和丙烯的物质的量共1mol,完成燃烧生成3molH2O | |
| C. | 1-丙醇和2-丙醇的一氯代物种类不同 | |
| D. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 |


 ;
;