题目内容
20.锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH-+2H2O═2Zn(OH)${\;}_{4}^{2-}$.下列说法正确的是( )| A. | 充电时,电解质溶液中K+向阳极移动 | |
| B. | 放电时,电解质溶液中K+向正极移动 | |
| C. | 充电时,阳极反应为:Zn(OH)${\;}_{4}^{2-}$+2e-═Zn+4OH- | |
| D. | 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况) |
分析 根据2Zn+O2+4OH-+2H2O═2Zn(OH)42-可知,O2中元素的化合价降低,被还原,应为原电池正极,Zn元素化合价升高,被氧化,应为原电池负极,充电时阳离子向阴极移动,放电时阳离子向正极移动,以此解答该题.
解答 解:A.充电时阳离子向阴极移动,即K+向阴极移动,故A错误;
B.放电时,为原电池,溶液中阳离子向正极移动,即K+向正极移动,故B正确;
C.充电时,阳极上发生失电子的氧化反应,阴极上发生得电子的氧化反应,则阴极反应为:Zn(OH)${\;}_{4}^{2-}$+2e-═Zn+4OH-,故C错误;
D.放电时,电路中通过4mol电子,消耗氧气1mol,其体积为22.4L(标准状况),故D错误.
故选B.
点评 本题考查原电池与电解池的基础知识,正确判断正负极、阴阳极,注意电极反应式的书写及电子转移的计算,正确判断化合价的变化为解答该题的关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.酸雨的pH小于5.6,下列气体排放会形成酸雨的是( )
| A. | N2 | B. | CO2 | C. | SO2 | D. | 氟氯代烷 |
5.化学与生活密切相关,下列说法不正确的是( )
| A. | 葡萄糖可用于补钙药物的合成 | |
| B. | 次氯酸钠溶液可用于环境的消毒杀菌 | |
| C. | 聚乙烯塑料制品可用于食品的包装 | |
| D. | 生石灰可用作食品抗氧剂 |
9.表是元素周期表一部分,列出了十个元素在周期表中的位置:
请用化学用语回答下列问题:
(1)在①~⑦元素中,原子半径最大的是K(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),⑤所对应元素的单质工业制备方法为2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
(3)用电子式表示元素③与⑧形成化合物的过程 .
.
(4)我国首创以单质⑤-空气-海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使单质⑤不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光.则电源的负极反应是4Al-12e-=4Al3+,正极反应为3O2+6H2O+12e-=12OH-.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | |||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ④ | ⑨ |
(1)在①~⑦元素中,原子半径最大的是K(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),⑤所对应元素的单质工业制备方法为2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
(3)用电子式表示元素③与⑧形成化合物的过程
 .
.(4)我国首创以单质⑤-空气-海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使单质⑤不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光.则电源的负极反应是4Al-12e-=4Al3+,正极反应为3O2+6H2O+12e-=12OH-.
7.相对分子质量为100的饱和链状烷烃,同分异构体中主链有5个原子的有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
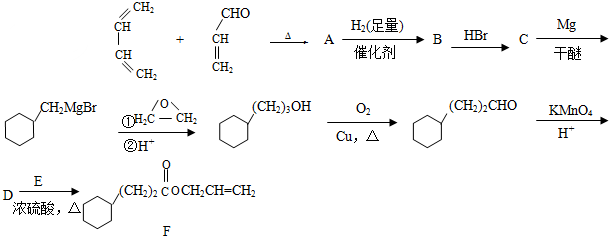
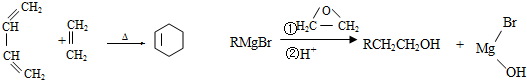
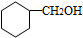 .
. .
. .
.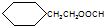
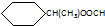 .
.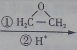 CH3CH2CH2CH2OH(其他试剂任选).
CH3CH2CH2CH2OH(其他试剂任选).