题目内容
(8分) 某透明澄清溶液可能含有Na+、Fe3+、Ba2+、CO32-、SO32-、SO42-、Cl-、I-等离子中的几种,为鉴别这些离子,分别取三份少量溶液,按照以下顺序进行三个实验:
实验①:加CCl4,再滴加少量氯水,振荡后,CCl4后层变为紫色;
实验②:加盐酸后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
实验③:加BaCl2溶液产生白色沉淀,过滤出沉淀,在沉淀中加入足量盐酸,沉淀不能完全溶解。
(1)分析上述3个实验,用离子符号写出每一个实验得出的结论,可不必完全填满。
实验①:含有 ;不含 ;
实验②:含有 ;不含 ;
实验③:含有 ;
(2)通过上述实验,不能确定是否存在的离子是 。
(1)① 含有I-;不含Fe3+; ② 含有CO32-、Na+;不含SO32- 和Ba2+;
③ 含有SO42-(1分,可以答成“含有CO32-和SO42-”,其他答案不得分)
(2)Cl- (1分)。
【解析】
试题分析:(1)①实验①:加CCl4,再滴加少量氯水,振荡后,CCl4后层变为紫色;则该溶液中含有I-;由于I-与Fe3+会发生反应:2Fe3++2I-= I2+2Fe2+而不能大量共存,所以一定不含有含Fe3+;实验②:加盐酸后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊,则该气体是CO2,原溶液中含有CO32-、不含有SO32-;由于CO32-与Fe3+、Ba2+会发生沉淀反应而不能大量共存,但是根据溶液呈电中性的原理可知该溶液中还应该含有离子Na+;所以该溶液中含有CO32-、Na+;不含SO32- 和Ba2+;实验③:加BaCl2溶液产生白色沉淀,过滤出沉淀,在沉淀中加入足量盐酸,沉淀不能完全溶解,则该溶液中含有CO32-、SO42-。(2)通过上述实验,可知一定含有的离子是Na+、CO32-、I-、SO42-;一定不含有的离子是Fe3+、Ba2+、SO32-,而不能确定是否存在的离子是Cl-。
考点:考查溶液中离子的存在的检验的知识。

 ② NH4Cl电子式:
② NH4Cl电子式: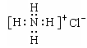
 ④ 丙烷分子的球棍模型:
④ 丙烷分子的球棍模型:
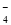
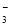 的水溶液中:NH
的水溶液中:NH 、Fe2+、SO
、Fe2+、SO 、H+
、H+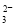 、Br-
、Br-
 B+2C+2D。测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
B+2C+2D。测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为( )