题目内容
17.用pH大小表示溶液的酸碱性相对强弱有许多不足之处,因此,荷兰科学家Hcnk Van Lubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为c(H+)与c(OH-)比值的对数,酸度的计算公式表示为AG=lg[c(H+)/c(OH-)],常温下,在AG=1的溶液中能大量共存的离子是( )| A. | Ca2+、K+、Cl-、NO3- | B. | NH4+、Fe3+、I-、SO42- | ||
| C. | Na+、K+、ClO-、S2- | D. | Na+、S2O32-、AlO2-、K+ |
分析 AG=lg[c(H+)/c(OH-)],常温下,在AG=1的溶液中,c(H+)/c(OH-)=0.1,溶液显碱性,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:A.碱性溶液中不能大量存在Ca2+,故A不选;
B.Fe3+、I-发生氧化还原反应,且碱性溶液中不能大量存在NH4+、Fe3+,故B不选;
C.ClO-、S2-发生氧化还原反应,故C不选;
D.碱性溶液中该组离子之间不反应,可大量共存,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
7.下列关于物质用途的叙述中正确的是( )
| A. | 镁合金的硬度比镁小 | |
| B. | 推广使用无磷洗衣粉主要是为了防止水体富营养化 | |
| C. | 纯碱可作治疗胃酸过多的一种药剂 | |
| D. | SO2可用于漂白一切有色物质 |
8.分类是化学研究中常用的方法.下列分类方法中不正确的是( )
| A. | 依据分子中含有氢原子的数目,将酸分为一元酸、二元酸等 | |
| B. | 依据是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素 | |
| D. | 根据分散质粒子直径的大小,将分散系分为浊液、胶体和溶液 |
5.已知酸性强弱顺序为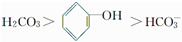 ,则下列化学方程式中正确的是( )
,则下列化学方程式中正确的是( )

 ,则下列化学方程式中正确的是( )
,则下列化学方程式中正确的是( )
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
12.把石蕊试液滴加到新制的氯水中,对其出现的现象描述正确的是( )
| A. | 溶液变红色 | B. | 溶液变蓝色 | ||
| C. | 溶液变紫色 | D. | 溶液颜色先变红后立即消失 |
9.在碱性溶液中能大量共存且为无色透明的溶液是( )
| A. | K、Cl-、MnO4-、SO42- | B. | Na+、SiO32-、NO3-、CO32- | ||
| C. | Na+、NO3-、SO42-、HCO3- | D. | Na+、SO42-、HS-、Cl- |
6.铝合金、氧化铝、硫酸铝三种物质的分类正确的是( )
| A. | 混合物、氧化物、盐 | B. | 单质、混合物、盐 | ||
| C. | 盐、氧化物、纯净物 | D. | 混合物、盐、化合物 |
16.有关化学键的断裂和形成,下列说法正确的是( )
| A. | 氢气在氧气中燃烧时,存在化学键的断裂和形成 | |
| B. | 有化学键断裂的过程一定是化学变化 | |
| C. | 化学反应过程中,所有反应物中都要断裂化学键 | |
| D. | 干冰升华时,分子中的共价键发生断裂 |
 .
. .
. .
. .
.