题目内容
14.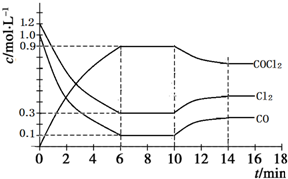 在1L恒容密闭容器中发生如下反应:Cl2(g)+CO(g)?COCl2(g)△H<0,图为容器内各物质的浓度随时间变化的曲线.下列说法不正确的是( )
在1L恒容密闭容器中发生如下反应:Cl2(g)+CO(g)?COCl2(g)△H<0,图为容器内各物质的浓度随时间变化的曲线.下列说法不正确的是( )| A. | 0~6 min内,反应的平均速率v(Cl2)=0.15mol•L-1•min-1 | |
| B. | 由图可知,第10 min时改变的外界条件是升温 | |
| C. | 保持温度不变,第8 min 时加入体系中的三种物质各1 mol,则平衡向逆反应方向移动 | |
| D. | 保持温度不变,若第10 min时向容器中再充入0.6 molCl2、0.5 molCO,则Cl2转化率增大 |
分析 A、由图可知,6min时Cl2的平衡浓度为0.3mol/L,浓度变化为1.2mol/L-0.3mol/L=0.9mol/L,据v=$\frac{△c}{△t}$计算;
B、由图可知,第10 min时平衡逆向移动,据影响平衡移动的3因素分析;
C、原平衡时n(Cl2):n(CO):n(COCl2)=3:1:9,现在第8 min 加入体系中的三种物质各1mol,则反应物的浓度增大程度大些,平衡正向移动;
D、原平衡时n(Cl2):n(CO):n(COCl2)=3:1:9,若第10 min时向容器中再充入0.6 molCl2、0.5 molCO,CO增大的比例大,则Cl2转化率增大.
解答 解:A、由图可知,6min时Cl2的平衡浓度为0.3mol/L,浓度变化为1.2mol/L-0.3mol/L=0.9mol/L,则v(Cl2)=$\frac{0.9mol/L}{6min}$=0.15 mol•L-1•min -1,故A正确;
B、影响平衡移动的因素有温度、浓度和压强,该反应是放热反应,由图可知,第10 min时平衡逆向移动,只能是升温,故B正确;
C、原平衡时n(Cl2):n(CO):n(COCl2)=3:1:9,现在第8 min 加入体系中的三种物质各1mol,则反应物的浓度增大程度大些,平衡正向移动,故C错误;
D、原平衡时n(Cl2):n(CO):n(COCl2)=3:1:9,若第10 min时向容器中再充入0.6 molCl2、0.5 molCO,CO增大的比例大,则Cl2转化率增大,故D正确;
故选C.
点评 本题考查了化学反应速率的求算、影响平衡移动的因素以及转化率的相关知识,题目难度不大,易错点是D,注意平衡时各物质的物质的量之比.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
5.可逆反应:2A+2B?C+3D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
| A. | v(A)=0.0075 mol•L-1•min-1 | B. | v(B)=0.01 mol•L-1•mim-1 | ||
| C. | v(C)=0.5 mol•L-1•s-1 | D. | v(D)=0.4 mol•L-1•s-1 |
9.对于反应中的能量变化,表述正确的是( )
| A. | 氧化反应均为吸热反应 | |
| B. | 断开化学键的过程会放出能量 | |
| C. | 加热才能发生的反应一定是吸热反应 | |
| D. | 放热反应中,反应物的总能量大于生成物的总能量 |
19.下列行为符合安全要求的是( )
| A. | 浓硫酸粘到皮肤上立即用稀氢氧化钠溶液冲洗 | |
| B. | 配制稀硫酸时将水倒入浓硫酸中 | |
| C. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| D. | 金属钠着火时,立即用砂子灭火 |
6.下列说法错误的是( )
| A. | HF可以用于刻蚀玻璃 | |
| B. | 用小苏打(NaHCO3)发酵面团制作馒头 | |
| C. | SO2具有漂白性,可用于漂白纸浆,也可以大量用于漂白食品 | |
| D. | 纯碱用于生产普通玻璃,也可用纯碱溶液来除去物品表面的油污 |
3.生活中常用84消毒液杀菌消毒,已知:向NaOH溶液中通入Cl2可制得84消毒液.下列有关说法不正确的( )
| A. | 制备84消毒液的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O | |
| B. | 84消毒液的有效成分是NaCl、NaClO | |
| C. | 84消毒液在空气中放置一段时间还可以用来漂白衣物 | |
| D. | 84消毒液与洁厕剂(主要成分:盐酸)不能一起使用 |
4.下列表达方式错误的是( )
| A. | HCl的电子式:H:Cl | |
| B. | S2-离子的电子层结构: | |
| C. | 质量数为18的氧元素的核素:${\;}_{8}^{18}$O | |
| D. | CO2的结构式:O=C=O |