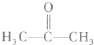
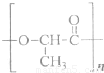
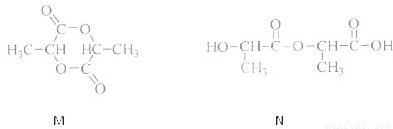题目内容
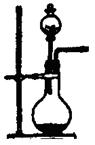
如图中,A是氯气的发生装置,B、C是净化气体的装置,D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置.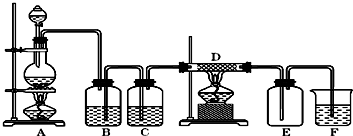
(1)上述装置中有一处错误,请指出是
(2)通过B是为了除去
(3)写出D、F中发生反应的化学方程式
(4)如果A中产生氯气3.36L(标准状况),请计算:A中的反应为(MnO2+4HCl(浓)
| ||
分析:(1)洗气装置的导气管要遵循“长进短出”的原则;
(2)浓盐酸具有挥发性,气体通过水溶液时会带出部分水蒸气,所以制取的氯气中含有氯化氢、水蒸气,要出去氯化氢和水蒸气,再让干燥的氯气和铁反应;
(3)在加热条件下,铁和氯气反应生成氯化铁;氯气和氢氧化钠反应生成氯化钠、次氯酸钠;
(4)根据氯气和二氧化锰之间的关系式计算二氧化锰消耗的物质的量,根据原子守恒计算被氧化的HCl的物质的量.
(2)浓盐酸具有挥发性,气体通过水溶液时会带出部分水蒸气,所以制取的氯气中含有氯化氢、水蒸气,要出去氯化氢和水蒸气,再让干燥的氯气和铁反应;
(3)在加热条件下,铁和氯气反应生成氯化铁;氯气和氢氧化钠反应生成氯化钠、次氯酸钠;
(4)根据氯气和二氧化锰之间的关系式计算二氧化锰消耗的物质的量,根据原子守恒计算被氧化的HCl的物质的量.
解答:解:(1)洗气装置的导气管要遵循“长进短出”的原则,所以错误地方为B,故答案为:B;
(2)浓盐酸具有挥发性,气体通过水溶液时会带出部分水蒸气,所以制取的氯气中含有氯化氢、水蒸气,要出去氯化氢和水蒸气,再让干燥的氯气和铁反应,用饱和食盐水除去氯化氢,用浓硫酸除去水蒸气,
因为饱和食盐水中含有水,所以应该先除去氯化氢再除去水蒸气,故答案为:HCl;饱和食盐水;水蒸气;
(3)在加热条件下,铁和氯气反应生成氯化铁,反应方程式为:3Fe+3Cl2
2FeCl3;氯气和氢氧化钠反应生成氯化钠、次氯酸钠,反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:3Fe+3Cl2
2FeCl3;Cl2+2NaOH=NaCl+NaClO+H2O;
(4)设消耗二氧化锰的物质的量为x,
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
1mol 22.4L
x 3.36L
1mol:22.4L=x:3.36L
x=
=0.15mol,
根据原子守恒知,被氧化的n(HCl)=2n(Cl2)=2×
=0.3mol,
故答案为:0.15mol;0.3mol.
(2)浓盐酸具有挥发性,气体通过水溶液时会带出部分水蒸气,所以制取的氯气中含有氯化氢、水蒸气,要出去氯化氢和水蒸气,再让干燥的氯气和铁反应,用饱和食盐水除去氯化氢,用浓硫酸除去水蒸气,
因为饱和食盐水中含有水,所以应该先除去氯化氢再除去水蒸气,故答案为:HCl;饱和食盐水;水蒸气;
(3)在加热条件下,铁和氯气反应生成氯化铁,反应方程式为:3Fe+3Cl2
| ||
| ||
(4)设消耗二氧化锰的物质的量为x,
MnO2+4HCl(浓)
| ||
1mol 22.4L
x 3.36L
1mol:22.4L=x:3.36L
x=
| 1mol×3.36L |
| 22.4L |
根据原子守恒知,被氧化的n(HCl)=2n(Cl2)=2×
| 3.36L |
| 22.4L/mol |
故答案为:0.15mol;0.3mol.
点评:本题考查了氯气的制取、除杂、干燥、收集及物质的量的计算等知识点,根据物质的性质选取除杂、干燥、收集所用试剂,再结合物质之间的关系式进行有关计算,难度不大.

练习册系列答案
相关题目
实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
|
编号 |
A |
B |
C |
|
发 生 装 置 |
|
|
|
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是 (写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是 (写编号),写出微热时的反应方程式 ;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 ↑ +
8H2O
2KCl + 2MnCl2 + 5Cl2 ↑ +
8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中 元素被氧化, 是氧化剂。当有1mol电子转移时,可生成气体 升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示:

写出圆底烧瓶中发生反应的化学方程式_
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.

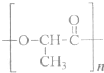

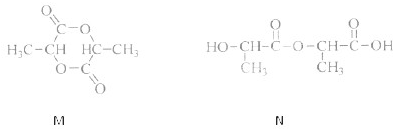
 (1)消毒液的主要成分是________(填化学式).
(1)消毒液的主要成分是________(填化学式).