题目内容
配制100mL、1.0mol?L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是( )
| A、读数时,俯视确定凹液面与刻度线相切 |
| B、容量瓶使用前经蒸馏水清洗后还残留有少量蒸馏水 |
| C、定容后把容量瓶颠倒摇匀,发现液面低于刻度线,又补足了所缺的水 |
| D、配制过程中,用蒸馏水洗涤烧杯和玻璃棒后,未把洗涤液移入容量瓶 |
考点:配制一定物质的量浓度的溶液
专题:
分析:分析具体操作对溶质的物质的量或对溶液的体积的影响,根据c=
进行具体判断.
| n |
| V |
解答:
解:A、定容时俯视凹液面,导致所配溶液的体积偏小,所配溶液浓度偏高,故A符合.
B、配制最后需加水定容,故容量瓶使用前有少量蒸馏水,对所配溶液浓度无影响,故B不符合;
C、定容后把容量瓶颠倒摇匀,发现液面低于刻度线,又补足了所缺的水,导致所配溶液体积偏大,所配溶液浓度偏低,故C不符合;
D、少量氢氧化钠粘在烧杯壁和玻璃棒上,未把洗涤液移入容量瓶,移入容量瓶内氢氧化钠的物质的量减小,所配溶液浓度偏低,故D不符合;
故选:A.
B、配制最后需加水定容,故容量瓶使用前有少量蒸馏水,对所配溶液浓度无影响,故B不符合;
C、定容后把容量瓶颠倒摇匀,发现液面低于刻度线,又补足了所缺的水,导致所配溶液体积偏大,所配溶液浓度偏低,故C不符合;
D、少量氢氧化钠粘在烧杯壁和玻璃棒上,未把洗涤液移入容量瓶,移入容量瓶内氢氧化钠的物质的量减小,所配溶液浓度偏低,故D不符合;
故选:A.
点评:本题考查了一定物质的量浓度溶液的配制,难度不大,误差分析关键关键清楚溶液配制原理.分析不当操作对n或V的影响,通过c=
进行计算判断.
| n |
| V |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质:①MgCl2 ②SiO2 ③白磷 ④BF3 ⑤NH3 ⑥四氯化碳 其中含极性键的非极性分子是( )
| A、①②③④⑥ | B、①④⑤⑥ |
| C、③④⑥ | D、④⑥ |
升高温度时,化学反应速率加快,主要原因是( )
| A、分子运动速率加快,使该反应物分子的碰撞机会增多 |
| B、反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C、该化学反应的过程是吸热的 |
| D、该化学反应的过程是放热的 |
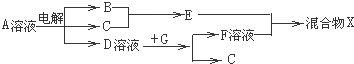
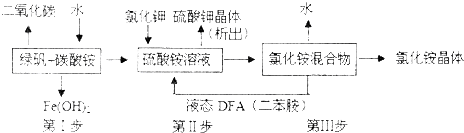
强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32-、SO32-、SO42-、C1-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下:下列结论正确的是( )


| A、X中不能确定的离子是 A13+、Na+、K+和C1- |
| B、气体F经催化氧化可直接生成气体D |
| C、沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 |
| D、X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- |
化学平衡常数K的数值大小是衡量化学反应进行程度的标志.在常温下,下列反应的平衡常数的数值如下:以下说法正确的是( )
2NO(g)?N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g)?2H2O(l) K2=2×1081
2CO2(g)?2CO(g)+O2(g) K3=4×10-92.
2NO(g)?N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g)?2H2O(l) K2=2×1081
2CO2(g)?2CO(g)+O2(g) K3=4×10-92.
| A、常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)?c(O2) |
| B、常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C、常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D、以上说法都不正确 |