题目内容
下列物质中,是强电解质的是( )
| A、二氧化碳气体 | B、固体氯化钠 |
| C、蔗糖溶液 | D、盐酸 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
解答:
解:A.二氧化碳气体自身不能电离,是非电解质,故A错误;
B.固体氯化钠在水溶液中完全电离,是强电解质,故B正确;
C.蔗糖溶液是混合物,既不是电解质也不是非电解质,故C错误;
D.盐酸是混合物,既不是电解质也不是非电解质,故D错误;
故选B.
B.固体氯化钠在水溶液中完全电离,是强电解质,故B正确;
C.蔗糖溶液是混合物,既不是电解质也不是非电解质,故C错误;
D.盐酸是混合物,既不是电解质也不是非电解质,故D错误;
故选B.
点评:本题考查电解质、非电解质、强弱电解质概念的辨析,难度不大.解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件.

练习册系列答案
相关题目
高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是 ( )
| A、浓硝酸 | B、硝酸银 |
| C、氯水 | D、纯碱 |
 X、Y、Z、W四种短周期元素在周期表中的位置如图所示.已知这四种元素原子的核电荷数之和为36.则这四种元素按X、Y、Z、W顺序依次是( )
X、Y、Z、W四种短周期元素在周期表中的位置如图所示.已知这四种元素原子的核电荷数之和为36.则这四种元素按X、Y、Z、W顺序依次是( )| A、N、P、O、C |
| B、C、N、O、P |
| C、O、S、N、F |
| D、C、Si、Al、N |
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A、一定有Cl- |
| B、一定有SO42- |
| C、一定没有Al3+ |
| D、一定有CO32- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴人酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO42- |
| B、能使红色石蕊试纸变蓝色的溶液中:K+、CO32-、NO3-、AlO2- |
| C、水电离产生的.(H+)=10-13mol/L的溶液中:Na+、Cl-、NO3-、CH3 COO- |
| D、pH=l 的溶液中:Na+、Fe2+、NO3-、Cl- |
下列实验操作或装置正确的是( )
A、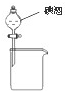 碘酒中的碘和酒精 |
B、 实验室制氨气 |
C、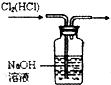 除去Cl2中的HCl |
D、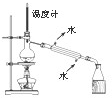 实验室制蒸馏水 |
将过量的SO2气体通入下列溶液中,最终没有沉淀的是( )
| A、Na[Al(OH)4] |
| B、BaCl2 |
| C、Ba(NO3)2 |
| D、Na2SiO3 |
下列反应属于放热反应的是( )
A、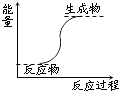 能量变化如图所示的反应 |
| B、燃烧反应和铝热反应 |
| C、化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D、氢氧化钡晶体和氯化铵晶体的反应 |
 一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )
一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )