题目内容
在2升的密闭容器中,发生以下反应:2A(g)+B(g)  2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速率为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速率为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
A.1.6 mol B.2.8 mol C.2.4 mol D.1.2 mol
B
【解析】
试题分析:根据速率之比等于化学计量数之比,所以v(B)=0.5v(A)=0.5×0.12mol/(L?s)=0.06mol/(L?s),所以△c(B)=0.06mol/(L?s)×10s=0.6mol/L,所以△n(B)=0.6mol/L×2L=1.2mol,故10秒钟时容器中B的物质的量为4mol-1.2mol=2.8mol;答案选B。
考点:考查化学反应速率的相关计算。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列化学用语正确的是( )
A、CO2的比例模型: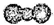 |
B、氢化铵(NH4H)电子式: |
C、氮气电子式 |
| D、O-18的原子符号:818O |