题目内容
16. 氨在化肥生产、制冷、“贮氢”及燃煤烟气脱硝脱硫等领域用途非常广泛.
氨在化肥生产、制冷、“贮氢”及燃煤烟气脱硝脱硫等领域用途非常广泛.(1)尿素[OC(NH2)2]与氰酸铵(NH4CNO)互为同分异构体;氰酸铵属于离子 (选填“离子”或“共价”)化合物.
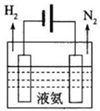
(2)液氨是一种重要的制冷剂,制冷过程中气态氨转变为液氨将释放 (选填“吸收”或“释放“)能童.液氨也是一种“贮氢”材料,液氨可通过如图装置释放氢气,该过程中能童转化方式为电能转化为化学能.
(3)已知拆开1mol气态物质中某种共价键需要吸收的能星就是该共价键的键能,某些共价键的键能见下表:
| 共价键 | H-H | N-H | N=N |
| 键能/kJ•mol-1 | 436 | 390.8 | 946 |
(4)氨气可作为脱硝剂.在恒温恒容密闭荇器中充入NO和NH3,在一定条件下发生了反 应:6NO(g)+4NH3(g)=5N2(g)+6H2O(g).已知反应开始时NO的物质的量浓度是1.2mol•L-1,2min后,NH3的物质的量浓度从开始的1.0mol•L-1降到 0.8mol•L-1,则
①2min末NO的物质的量浓度为0.9mol/L.
②这2min内N2的平均反应速率为0.125mol/(L•min).
(5)工业上用氨水吸收硫酸工业尾气中的SO2,既可消除污染又可获得NH4HSO3等产品. 若用1000kg含NH3质量分数为17%的氨水吸收SO2且全部转化为NH4HSO3,不考虑其它成本,则可获得的利润为782元(参照下面的价格表).
| NH3质量分数17%的氨水 | 无水 NH4HSO3 | |
| 价格(元/kg) | 1.0 | 1.8 |
分析 (1)分子式相同结构不同的化合物属于同分异构体;氰酸铵属于盐;
(2)气态转化为液态释放能量,电解是电能转化为化学能;
(3)化学反应中旧键断裂需要吸收能量,新键形成需要放出能量,化学反应中的反应热△H=反应物总键能-生成物总键能;
(4)各个物质的浓度变化量之比等于物质前边的系数之比;不同物质表示的速率之比等于系数之比;
(5)根据SO2+NH3+H2O=NH4HSO3进行计算.
解答 解:(1)氰酸铵(NH4OCN)与尿素[CO(NH2)2]的分子式相同但结构不同,所以属于同分异构体;氰酸铵属于盐,是离子化合物,故答案为:同分异构体;离子;
(2)气态氨转化为液态释放能量,图1装置为电解装置,电解是电能转化为化学能,故答案为:释放;电能转化为化学能;
(3)化学反应中的反应热△H=反应物总键能-生成物总键能=946+436×3-390.8×6=:-90.8kJ•mol-1,故答案为:-90.8;
(4)①NH3的物质的量浓度从开始的1.0mol•L-1降到 0.8mol•L-1,则减少了0.2mol/L,所以NO的浓度会减少0.3mol/L,2min末NO的物质的量浓度为1.2mol/L-0.3mol/L=0.9mol/L,故答案为:0.9mol/L;
②NH3的物质的量浓度从开始的1.0mol•L-1降到 0.8mol•L-1,则减少了0.2mol/L,这2min内氨气的平均反应速率为0.1mol/L,N2的平均反应速率为$\frac{5}{4}$×0.1mol/L=0.125mol/L,故答案为:0.125mol/(L•min),故答案为:0.125mol/(L•min);
(5)1000kg×17%=170kg,设无水NH4HSO3的质量为X.
SO2+NH3+H2O=NH4HSO3
17 99
170kg X
$\frac{17}{170kg}$=$\frac{99}{x}$,解得X=990kg,990×1.8-1000=782,故答案为:782.
点评 本题考查化学平衡状态、反应热以及化学方程式的计算等,题目难度中等,注意化学反应中的反应热△H=反应物总键能-生成物总键能.

| A. | 过量的铜与浓硝酸反应有一氧化氮生成 | |
| B. | Al、Fe、Cu的单质放置在空气中均只生成氧化物 | |
| C. | SiO2与酸、碱均不反应 | |
| D. | 向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,则H2SiO3的酸性比H2CO3的酸性强 |
| A. | 活化分子的能量不变 | B. | 增加了活化分子的百分数 | ||
| C. | 降低了反应的活化能 | D. | 改变了化学反应的能量变化 |
| 时间(s) | 0 | 4 | 8 | 12 | 16 | 20 |
| n(N2O4)(mol) | 0.40 | a | 0.20 | c | d | e |
| n(NO2)(mol) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)在80℃时该反应的平衡常数K=3.6mol/L.
(3)要增大该反应的平衡常数,可采取的措施有④(填序号).
①增大N2O4的起始浓度 ②向混合气体中通入NO2
③使用高效催化剂 ④升高温度
(4)反应进行至20s后若降低温度,混合气体的颜色变浅(填“变浅”、“变深”或“不变”).
(5)反应进行至20s后若向容器中再充入0.40mol的N2O4气体,则达到新平衡后N2O4的转化率将减小(选填“增大”、“减小”或“不变”).
| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加入AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加入足量NaOH溶液并加热 | 收集到气体0.896L(换算成标准状况) |
| 3 | 加入足量BaCl2溶液,将所得沉淀洗涤、干燥、称重;再向沉淀中加足量的稀盐酸,洗涤、干燥、称重 | 第一次称重读数为6.27g,第二次称重读数为2.33g |
(1)判断混合物中Cl-是否一定存在否.(填“是”或“否”)
(2)写出溶液中一定存在的离子及其物质的量浓度:c(SO42-)=0.1mol/L、c(CO32-)=0.2mol/L、c(NH4+)=0.4mol/L、c(K+)≥0.2mol/L.
| A. | v(SO2)=4mol•L-1•min-1 | B. | v(O2)=3mol•L-1•min-1 | ||
| C. | v(SO2)=0.1mol•L-1•s-1 | D. | v(O2)=0.1mol•L-1•s-1 |
 .
.