题目内容
| 实验要求 | 选用的试剂 | 涉及的离子方程式 |
| 除去氢氧化镁中的氢氧化铝杂质 | ||
| 除去FeCl2溶液中FeCl3 | ||
| 鉴别炭粉和氧化铜 |
考点:离子方程式的书写,物质的分离、提纯的基本方法选择与应用
专题:离子反应专题
分析:氢氧化镁不溶于强碱、氢氧化铝能溶于强碱,所以用NaOH溶液除去氢氧化铝;
铁离子能被铁还原生成亚铁离子;
氧化铜能和稀盐酸反应、C和稀盐酸不反应,所以用稀盐酸鉴别氧化铜和C.
铁离子能被铁还原生成亚铁离子;
氧化铜能和稀盐酸反应、C和稀盐酸不反应,所以用稀盐酸鉴别氧化铜和C.
解答:
解:氢氧化镁不溶于强碱、氢氧化铝能溶于强碱,所以用NaOH溶液除去氢氧化铝,离子方程式为Al(OH)3+OH-=AlO2-+2H2O;
铁离子和铁反应生成亚铁离子,所以可以用铁粉除去氯化铁,离子方程式为2Fe3++Fe=3Fe2+;
氧化铜能和稀盐酸反应、C和稀盐酸不反应,所以用稀盐酸鉴别氧化铜和C,离子方程式为CuO+2H+=Cu2++H2O,
故答案为:
.
铁离子和铁反应生成亚铁离子,所以可以用铁粉除去氯化铁,离子方程式为2Fe3++Fe=3Fe2+;
氧化铜能和稀盐酸反应、C和稀盐酸不反应,所以用稀盐酸鉴别氧化铜和C,离子方程式为CuO+2H+=Cu2++H2O,
故答案为:
| 实验要求 | 选用的试剂 | 涉及的离子方程式 |
| 除去氢氧化镁中的氢氧化铝杂质 | NaOH溶液 | Al(OH)3+OH-=AlO2-+2H2O |
| 除去FeCl2溶液中FeCl3 | Fe | 2Fe3++Fe=3Fe2+ |
| 鉴别炭粉和氧化铜 | 盐酸 | CuO+2H+=Cu2++H2O |
点评:本题以除杂为载体考查了离子方程式的书写,明确物质的性质及除杂原则是解本题关键,除杂时不能引进新的杂质,难点是除杂剂的选取,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 纽约一家公司设计出Soccket足球,每被踢一下,足球的内置机制就会把能量储存起来;被储存的能量可以通过USB接口给手机或其他小家电充电.在Soccket足球充放电的过程中,能量转化的主要形式是( )
纽约一家公司设计出Soccket足球,每被踢一下,足球的内置机制就会把能量储存起来;被储存的能量可以通过USB接口给手机或其他小家电充电.在Soccket足球充放电的过程中,能量转化的主要形式是( )| A、电能→化学能→电能 |
| B、化学能→电能→化学能 |
| C、机械能→电能→化学能 |
| D、机械能→化学能→电能 |
已知:
①1mol H2分子中化学键断裂时需要吸收436kJ的能量,
②1mol I2蒸气中化学键断裂时需要吸收151kJ的能量,
③由H原子和I原子形成1mol HI分子时释放299kJ的能量.
下列热化学方程式正确的是( )
①1mol H2分子中化学键断裂时需要吸收436kJ的能量,
②1mol I2蒸气中化学键断裂时需要吸收151kJ的能量,
③由H原子和I原子形成1mol HI分子时释放299kJ的能量.
下列热化学方程式正确的是( )
| A、2HI(g)=H2(g)+I2(g);△H=+11 kJ?mol-1 |
| B、H2(g)+I2(g)=HI(g);△H=-11 kJ?mol-1 |
| C、H2(g)+I2(g)=2HI(g);△H=+288 kJ?mol-1 |
| D、H2(g)+I2(g)=HI(g);△H=-114 kJ?mol-1 |
下列措施对增大反应速率明显有效的是( )
| A、Na与水反应时增大水的用量 | |||
| B、Fe与稀硫酸反应制取氢气时,改用浓硫酸 | |||
| C、在H2SO4与Na2CO3两溶液反应时,增大压强 | |||
D、反应N2+3H2
|
下列反应的离子方程式书写正确的是( )
| A、铁片放入稀盐酸中:Fe+2H+=Fe3++H2↑ |
| B、氢氧化铜与稀硫酸:OH-+H+=H2O |
| C、氯化钡溶液与硝酸银溶液:Cl-+Ag+=AgCl↓ |
| D、碳酸钙与稀硝酸:CO32-+2H+=CO2↑+H2O |
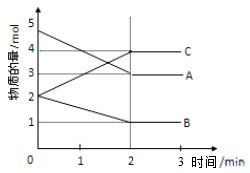 某温度时,在一恒容密闭容器中,A、B、C三种物质的物质的量n(mol)随时间t(min)变化的曲线如图所示,从图中的数据分析:
某温度时,在一恒容密闭容器中,A、B、C三种物质的物质的量n(mol)随时间t(min)变化的曲线如图所示,从图中的数据分析: (1)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.写出FeCl3溶液腐蚀印刷电路铜板的离子方程式
(1)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.写出FeCl3溶液腐蚀印刷电路铜板的离子方程式