题目内容
 I、向AlCl3溶液中滴加NaOH溶液至过量
I、向AlCl3溶液中滴加NaOH溶液至过量(1)实验现象
(2)相关反应离子方程式:
(3)完成图1(沉淀的物质的量与NaOH溶液体积的关系图)
II、向NaOH溶液中滴加AlCl3溶液至过量(1)实验现象
(2)反应离子方程式:
(3)完成图2(沉淀的物质的量与AlCl3溶液体积的关系图)
考点:镁、铝的重要化合物
专题:几种重要的金属及其化合物
分析:I、AlCl3中加入NaOH先生成Al(OH)3,发生3NaOH+AlCl3=Al(OH)3↓+3NaCl,Al(OH)3具有两性,可与NaOH反应生成NaAlO2,发生Al(OH)3+NaOH=NaAlO2+2H2O;
II、向NaOH溶液中滴加AlCl3溶液至过量,
II、向NaOH溶液中滴加AlCl3溶液至过量,
解答:
解:I、AlCl3中加入NaOH先生成Al(OH)3,发生Al3++3OH-═Al(OH)3↓,Al(OH)3具有两性,继续加入NaOH溶液则发生Al(OH)3+OH-═AlO2-+2H2O,可观察到沉淀溶解,
(1)向AlCl3溶液中滴加NaOH溶液至过量:先有白色沉淀产生,后来沉淀逐渐被溶解,直至完全消失;
故答案为:先有白色沉淀产生,后来沉淀逐渐被溶解,直至完全消失;
(2)向AlCl3溶液中滴加NaOH溶液至过量,先后发生反应:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O;
故答案为:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O;
(3)向氯化铝溶液中滴入NaOH溶液:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O,先产生沉淀,后沉淀溶解,而且所用NaOH溶液体积为3:1;
故答案为;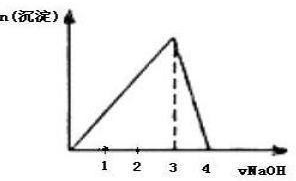
II、向NaOH溶液中滴加AlCl3溶液至过量,一开始NaOH是过量的,生成的Al(OH)3溶解在NaOH溶液中,生成NaAlO2,然后随着AlCl3的量的增多,当氢氧化钠反应完,再滴入的AlCl3和NaAlO2发生双水解,生成Al(OH)3沉淀,
(1)向NaOH溶液中滴加AlCl3溶液至过量,实验现象所以反应现象是:刚开始局部有白色沉淀产生,振荡后沉淀消失,后来又有白色沉淀产生,振荡后不再消失;
故答案为:刚开始局部有白色沉淀产生,振荡后沉淀消失,后来又有白色沉淀产生,振荡后不再消失;
(2)向NaOH溶液中滴加AlCl3溶液至过量,先后发生反应:Al3++4OH-=AlO2-+2H2O;3AlO2-+Al3++6H2O=4Al(OH)3↓;
故答案为:Al3++4OH-=AlO2-+2H2O;3AlO2-+Al3++6H2O=4Al(OH)3↓;
(3)向NaOH溶液中滴加AlCl3溶液至过量,先后发生反应:Al3++4OH-=AlO2-+2H2O;3AlO2-+Al3++6H2O=4Al(OH)3↓;先没有沉淀,后生成沉淀,且所用氯化铝体积比为3:1,
故答案为: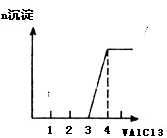
(1)向AlCl3溶液中滴加NaOH溶液至过量:先有白色沉淀产生,后来沉淀逐渐被溶解,直至完全消失;
故答案为:先有白色沉淀产生,后来沉淀逐渐被溶解,直至完全消失;
(2)向AlCl3溶液中滴加NaOH溶液至过量,先后发生反应:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O;
故答案为:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O;
(3)向氯化铝溶液中滴入NaOH溶液:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O,先产生沉淀,后沉淀溶解,而且所用NaOH溶液体积为3:1;
故答案为;

II、向NaOH溶液中滴加AlCl3溶液至过量,一开始NaOH是过量的,生成的Al(OH)3溶解在NaOH溶液中,生成NaAlO2,然后随着AlCl3的量的增多,当氢氧化钠反应完,再滴入的AlCl3和NaAlO2发生双水解,生成Al(OH)3沉淀,
(1)向NaOH溶液中滴加AlCl3溶液至过量,实验现象所以反应现象是:刚开始局部有白色沉淀产生,振荡后沉淀消失,后来又有白色沉淀产生,振荡后不再消失;
故答案为:刚开始局部有白色沉淀产生,振荡后沉淀消失,后来又有白色沉淀产生,振荡后不再消失;
(2)向NaOH溶液中滴加AlCl3溶液至过量,先后发生反应:Al3++4OH-=AlO2-+2H2O;3AlO2-+Al3++6H2O=4Al(OH)3↓;
故答案为:Al3++4OH-=AlO2-+2H2O;3AlO2-+Al3++6H2O=4Al(OH)3↓;
(3)向NaOH溶液中滴加AlCl3溶液至过量,先后发生反应:Al3++4OH-=AlO2-+2H2O;3AlO2-+Al3++6H2O=4Al(OH)3↓;先没有沉淀,后生成沉淀,且所用氯化铝体积比为3:1,
故答案为:

点评:本题考查:AlCl3溶液和NaOH溶液的反应,关键在于理解相关反应,熟练写出相应的反应的方程式,明确发生的化学反应及反应物的用量是解答的难点.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
巴豆酸的结构简式为CH3CH=CHCOOH 现有:①氯化氢,②溴水,③纯碱溶液,④酸性KMnO4溶液,⑤乙醇,试根据其结构特点,判断在一定条件下能与巴豆酸反应的物质组合是( )
| A、只有②④⑤ | B、只有①③④ |
| C、只有①②③ | D、都可以 |
已知镁粉与冷水几乎不反应,与热水反应缓慢.市场上购买的“即热饭盒”底部有两层,一层装水,另一层是镁粉与铁粉的混合物,当水与金属粉末接触时会发生反应:Mg+2H2O=Mg(OH)2+H2↑.则下列说法不正确的是( )
| A、“即热饭盒”的工作原理是将化学能转化为热能 |
| B、上述反应中,反应物的总能量大于生成物的总能量 |
| C、铁粉的作用是催化剂 |
| D、上述反应的反应热△H>0 |
充分燃烧一定量丁烷时放出的热量xQ,完全吸收它生成的CO2生成正盐,需5mol/L的KOH溶液100mL,则丁烷的燃烧热为( )
| A、16xQ | B、8xQ |
| C、4xQ | D、2xQ |
用食用白醋(醋酸浓度约1mol/L)常温下进行下列实验,能证明醋酸为弱电解质的是( )
| A、白醋中滴入石蕊试液呈红色 |
| B、实验测得该白醋的pH为2.3 |
| C、蛋壳浸泡在白醋中有气体放出 |
| D、白醋加入豆浆中有沉淀产生 |

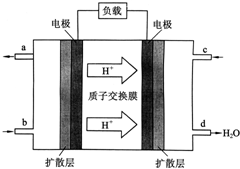 中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图所示.
中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图所示.