题目内容
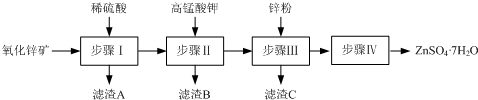
实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的主要实验流程如下.
(1)浸取时,为了加快浸取的速率又不增加成本,可以采用的措施是 .
(2)滤渣Ⅰ的成分为MnO2、单质S和 (写化学式);
(3)硫酸浸取时,Cu2S被MnO2氧化的化学方程式为 .
(4)浸取时,研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是 .
(5)“赶氨”时,最适宜的操作方法是 .
(6)“沉锰”发生反应的离子方程式为: .
(7)滤液Ⅱ经蒸发结晶得到的盐主要是 (写化学式).

(1)浸取时,为了加快浸取的速率又不增加成本,可以采用的措施是
(2)滤渣Ⅰ的成分为MnO2、单质S和
(3)硫酸浸取时,Cu2S被MnO2氧化的化学方程式为
(4)浸取时,研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是
(5)“赶氨”时,最适宜的操作方法是
(6)“沉锰”发生反应的离子方程式为:
(7)滤液Ⅱ经蒸发结晶得到的盐主要是
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:辉铜矿主要成分为Cu2S,含少量Fe2O3、SiO2等杂质,加入稀硫酸和二氧化锰浸取,过滤得到滤渣I为MnO2、SiO2、单质S,滤液中含有Fe3+、Mn2+、Cu2+,调节溶液PH除去铁离子,加入碳酸氢铵溶液沉淀锰离子,过滤得到滤液赶出氨气循环使用,得到碱式碳酸铜;
(1)根据影响反应速率的因素分析;
(2)分析流程结合物质性质可知二氧化硅不溶于稀硫酸溶液;
(3)硫化亚铜在酸溶液在被二氧化锰氧化生成硫酸铜,硫单质和硫酸锰;
(4)若先除铁再浸取,浸取速率明显变慢,Fe2O3在浸取时起媒介作用,Fe3+可催化Cu2S被MnO2氧化;
(5)“赶氨”时,最适宜的操作方法是减小氨气溶解度,加热驱赶;
(6)含有锰离子的溶液加碳酸氢铵和氨气,生成碳酸锰和碳酸铵;
(7)滤液Ⅱ主要是硫酸铵溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到硫酸铵晶体.
(1)根据影响反应速率的因素分析;
(2)分析流程结合物质性质可知二氧化硅不溶于稀硫酸溶液;
(3)硫化亚铜在酸溶液在被二氧化锰氧化生成硫酸铜,硫单质和硫酸锰;
(4)若先除铁再浸取,浸取速率明显变慢,Fe2O3在浸取时起媒介作用,Fe3+可催化Cu2S被MnO2氧化;
(5)“赶氨”时,最适宜的操作方法是减小氨气溶解度,加热驱赶;
(6)含有锰离子的溶液加碳酸氢铵和氨气,生成碳酸锰和碳酸铵;
(7)滤液Ⅱ主要是硫酸铵溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到硫酸铵晶体.
解答:
解:辉铜矿主要成分为Cu2S,含少量Fe2O3、SiO2等杂质,加入稀硫酸和二氧化锰浸取,过滤得到滤渣I为MnO2、SiO2、单质S,滤液中含有Fe3+、Mn2+、Cu2+,调节溶液PH除去铁离子,加入碳酸氢铵溶液沉淀锰离子,过滤得到滤液赶出氨气循环使用,得到碱式碳酸铜;
(1)固体与液体反应时增大固体的表面积可以加快反应速率,升高温度、增大硫酸浓度也能加快反应速率;
故答案为:将矿石粉碎(或提高浸取温度或适当增加酸的浓度等);
(2)分析流程结合物质性质可知二氧化硅不溶于稀硫酸溶液,在滤渣Ⅰ的成分为MnO2、单质S和SiO2;
故答案为:SiO2;
(3)硫化亚铜在酸溶液在被二氧化锰氧化生成硫酸铜,硫单质和硫酸锰,反应的化学方程式为:2MnO2+Cu2S+4H2SO4=2MnSO4+2CuSO4+S+4H2O,
故答案为:2MnO2+Cu2S+4H2SO4=2MnSO4+2CuSO4+S+4H2O;
(4)若先除铁再浸取,浸取速率明显变慢,Fe2O3在浸取时起媒介作用,Fe3+可催化Cu2S被MnO2氧化,
故答案为:Fe3+可催化Cu2S被MnO2氧化;
(5))“赶氨”时,最适宜的操作方法是减小氨气溶解度,可以加热驱赶,
故答案为:将溶液加热;
(6)含有锰离子的溶液加碳酸氢铵和氨气,生成碳酸锰和碳酸铵,其反应的离子方程式为:Mn2++HCO3-+NH3=MnCO3↓+CO32-+NH4+;
故答案为:Mn2++HCO3-+NH3=MnCO3↓+CO32-+NH4+;
(7)滤液Ⅱ主要是硫酸铵溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到硫酸铵晶体,故答案为:(NH4)2SO4.
(1)固体与液体反应时增大固体的表面积可以加快反应速率,升高温度、增大硫酸浓度也能加快反应速率;
故答案为:将矿石粉碎(或提高浸取温度或适当增加酸的浓度等);
(2)分析流程结合物质性质可知二氧化硅不溶于稀硫酸溶液,在滤渣Ⅰ的成分为MnO2、单质S和SiO2;
故答案为:SiO2;
(3)硫化亚铜在酸溶液在被二氧化锰氧化生成硫酸铜,硫单质和硫酸锰,反应的化学方程式为:2MnO2+Cu2S+4H2SO4=2MnSO4+2CuSO4+S+4H2O,
故答案为:2MnO2+Cu2S+4H2SO4=2MnSO4+2CuSO4+S+4H2O;
(4)若先除铁再浸取,浸取速率明显变慢,Fe2O3在浸取时起媒介作用,Fe3+可催化Cu2S被MnO2氧化,
故答案为:Fe3+可催化Cu2S被MnO2氧化;
(5))“赶氨”时,最适宜的操作方法是减小氨气溶解度,可以加热驱赶,
故答案为:将溶液加热;
(6)含有锰离子的溶液加碳酸氢铵和氨气,生成碳酸锰和碳酸铵,其反应的离子方程式为:Mn2++HCO3-+NH3=MnCO3↓+CO32-+NH4+;
故答案为:Mn2++HCO3-+NH3=MnCO3↓+CO32-+NH4+;
(7)滤液Ⅱ主要是硫酸铵溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到硫酸铵晶体,故答案为:(NH4)2SO4.
点评:本题考查了物质分离提纯的方法和流程分析应用,主要涉及物质性质的理解、影响速率的因素、离子方程式的书写等,掌握基础是关键,题目难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列有关电解质及氧化还原反应的叙述,正确的是( )
| A、某化合物溶于水导电,则该化合物为电解质 |
| B、NaCl溶液在电流作用下电离成Na+和Cl- |
| C、在氧化还原反应中,非金属单质一定是氧化剂 |
| D、元素由化合态变成游离态时,它可能被氧化,也可能被还原 |
在50mL 0.01mol?L-1下列溶液中,溶解CaCO3质量最大的是( )
| A、Na2CO3溶液 |
| B、NaOH溶液 |
| C、NH4Cl溶液 |
| D、NaHCO3溶液 |
已知常温下:KSP (AgCl)=1.8×10-10 mol2?L-2,KSP (Ag2CrO4)=1.9×10-12 mol3?L-3,下列叙述正确的是( )
| A、AgCl在饱和NaCl溶液中的 KSP比在纯水中的 KSP 小 |
| B、向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP (AgCl)<KSP (AgI) |
| C、将0.001 mol?L-1 的AgNO3溶液滴入0.001 mol?L-1 的KCl和0.001 mol?L-1 的K2CrO4 溶液中先产生Ag2CrO4沉淀 |
| D、向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
下列有关实验事实及其解释正确的是( )
| A、向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中含Fe2+ |
| B、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C、向某溶液中加入氯化钡溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,则原溶液一定含有SO42- |
| D、常温下,浓硫酸可以用铁质容器储运,说明铁与冷的浓硫酸不反应 |
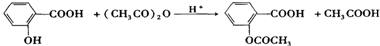
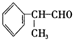 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下: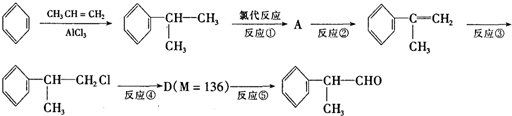
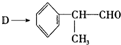 反应的化学方程式为
反应的化学方程式为