题目内容
15.某同学对未知物A盐的水溶液进行了鉴定,实验过程及现象如图所示: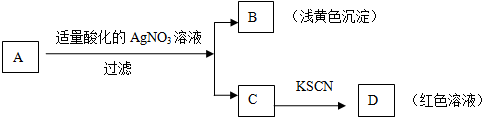
现对A、B、C、D作出的如下推断中,不正确的是( )
| A. | 盐A一定是FeBr3 | B. | 浅黄色沉淀B是AgBr | ||
| C. | 滤液C中一定含Fe 3+ | D. | D溶液中有Fe(SCN)3 |
分析 和硝酸银溶液发生反应生成淡黄色不溶于硝酸的沉淀时溴化银,三价铁离子遇到硫氰酸钾显示红色,据此分析作答;
解答 解:根据图示信息:未知物A盐的水溶液中加入酸化的硝酸银可以产生淡黄色沉淀溴化银,证明A中一定含有溴离子,C中加入硫氰酸钾显示红色,证明其中含有三价铁离子,该离子可以是二价铁离子被硝酸氧化来的,还可以是原来溶液中含有的.
A.盐A可以是FeBr3,还可以是FeBr2,故A错误;
B.浅黄色沉淀B是AgBr,故B正确;
C.C中加入硫氰酸钾显示红色,证明其中含有三价铁离子,故C正确;
D.三价铁离子和硫氰酸钾中的硫氰酸根离子发生反应会生成Fe(SCN)3,故D正确;
故选A.
点评 本题涉及亚铁离子和三价铁离子之间的检验知识,注意平时知识的积累是解题的关键,难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
3.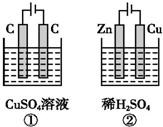 如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
 如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )| A. | 产生气体的总体积:①>② | |
| B. | 电极上析出物质的总质量:②>① | |
| C. | 溶液的pH变化:①增大,②减小 | |
| D. | ①中阳极的电极反应式:4OH--4e-═2H2O+O2↑;②中阴极的电极反应式:2H++2e-═H2↑ |
4.设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1mol•L-1K2SO4溶液中含有K+的数目为2NA | |
| B. | 标准状况下,2.24L氯仿(CHCl3)中含有C-Cl数目为0.3NA | |
| C. | 18g重水中所含有的中子数为10NA | |
| D. | 1molNa与O2在一条条件下反应生成Na2O和Na2O2的混合物的转移电子数为NA |
7.甲醛(CH2O)、乙酸(C2H4O2)和丙醛(C3H6O)组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为( )
| A. | 27% | B. | 28% | C. | 54% | D. | 无法计算 |
4.设NA为阿伏加德罗常数,下列说法中不正确的是( )
| A. | 标准状况下,密度为dg/L的某气体纯净物一个分子的质量为22.4d/NAg | |
| B. | 加热条件下,20mL10mol/L的浓硝酸与足量铜反应转移电子数为0.1NA | |
| C. | 电解精炼铜的过程中转移了NA个电子,则阴极析出32g铜 | |
| D. | 1L pH=1的硫酸溶液中,含有0.1NA个H+ |
5.化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A. | 绿色食品是生产时不使用化肥农药,不含任何化学物质的食品 | |
| B. | 加强化石燃料的开采利用,能从根本上解决能源危机 | |
| C. | 化学反应能够制造出新的物质,同时也能制造出新的元素 | |
| D. | 减少机动车尾气的排放,可以降低雾霾的发生 |
