题目内容
科学家P.Tatapudi等人首先使用在空气中电解纯水(酸性条件下)的方法制得臭氧.同时还得到了过氧化氢,下列电极反应式正确的是( )
| A、阳极反应:3O2+6H++6e-=3H2O2 |
| B、阳极反应:3H2O一6e-=O3+6H+ |
| C、阴极反应:3O2+6H2O+6e-=3H2O2+6OH- |
| D、阴极反应:3H2O一6e-=O3+6H+ |
考点:电极反应和电池反应方程式,原电池和电解池的工作原理
专题:电化学专题
分析:由阳极制得臭氧,阴极制得过氧化氢.电解总方程式为:3H2O+3O2═3H2O2+O3,阳极反应为3H2O→O3+6H++6e-,阴极反应为6H++3O2+6e-→3H2O2,以此来解答.
解答:
解:A、在电解池的阳极上发生失电子的氧化反应,不是得电子的反应,故A错误;
B、在电解池的阳极上发生失电子的氧化反应,即3H2O一6e-=O3+6H+,故B正确;
C、电解池的阴极上发生得电子的还原反应,即6H++3O2+6e-→3H2O2,在酸性环境下,不会出现氢氧根离子,故C错误;
D、电解池的阴极上发生得电子的还原反应,即6H++3O2+6e-→3H2O2,故D错误.
故选B.
B、在电解池的阳极上发生失电子的氧化反应,即3H2O一6e-=O3+6H+,故B正确;
C、电解池的阴极上发生得电子的还原反应,即6H++3O2+6e-→3H2O2,在酸性环境下,不会出现氢氧根离子,故C错误;
D、电解池的阴极上发生得电子的还原反应,即6H++3O2+6e-→3H2O2,故D错误.
故选B.
点评:本题为信息习题,考查电解原理,明确电解反应及阳极制得臭氧,阴极制得过氧化氢是解答本题的关键,难度不大.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、按化学家的观点来看:世界上没有真正的垃圾,只是放错了地方的资源 |
| B、尽管可充电电池的使用寿命相对较长,但这类电池仍须进行回收处理 |
| C、对医疗垃圾主要采取焚烧法进行处理,因病毒全部杀死,焚烧产物可任意排放 |
| D、商品过度包装及其一次性的大量使用,既增加了垃圾量又造成了资源的极大浪费 |
下列变化属于吸收能(热)量的是( )
| A、Cu+稀HNO3→ |
| B、H2O→H++OH- |
| C、CO→C+CO2 |
| D、H2+O2→H2O |
下列有关实验原理、装置、操作或结论的描述中,正确的是( )


| A、图①装置的烧杯中先出现白色沉淀后溶解 |
| B、图②装置可验证氧化性:ClO->Cl2>Fe3+ |
| C、图③装置可用于实验室制备乙烯 |
| D、图④装置可证明Na2CO3比NaHCO3更稳定 |
下列叙述正确的是( )
| A、硫酸钡难溶于水,在水溶液中不能导电,所以硫酸钡不是电解质 |
| B、强电解质在水溶液中的导电性一定比弱电解质强 |
| C、三氧化硫溶于水能导电,所以三氧化硫是电解质 |
| D、硫酸、氢氧化钡、纯碱、苛性钠都是强电解质 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4L CCl4含有NA个分子 |
| B、常温常压下46g NO2和N2O4混合气体含有3NA个原子 |
| C、0.1mol AlCl3完全转化为氢氧化铝胶体,生成0.lNA个胶体粒子 |
| D、0.1mol Cl2与足量NaOH溶液反应,转移电子数为0.2NA |
对于在恒温恒容容器中进行的反应A(g)+2B(g)?3C(g)+D(g),以下不能说明已达平衡状态的是
( )
( )
| A、反应容器中,压强不随时间改变而改变 |
| B、单位时间内生成3n mol C的同时生成n mol A |
| C、反应容器中,混合气体的平均相对分子质量不再改变 |
| D、反应容器中的气体密度不随时间变化 |
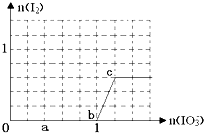 已知:还原性HSO3->I?,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )
已知:还原性HSO3->I?,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )| A、0-b:3HSO3-+IO3-═3SO42-+I-+3H+ |
| B、a点时消耗NaHSO3的物质的量为1.2mol |
| C、b-c间I2是还原产物 |
| D、当溶液中I?与I2的物质的量之比为5:2时,加入的KIO3为1.08mol |