题目内容
 第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.010mol?L-1的这四种溶液pH与该元素原子半径的关系如图所示.下列说法正确的是( )
第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.010mol?L-1的这四种溶液pH与该元素原子半径的关系如图所示.下列说法正确的是( )| A、气态氢化物的稳定性:Z>W>Y |
| B、简单离子半径:Z<W |
| C、Y元素存在同素异形体 |
| D、X和Y的最高价氧化物对应的水化物恰好中和时,溶液呈中性 |
考点:原子结构与元素周期律的关系,原子结构与元素的性质
专题:
分析:第三周期元素中,X最高价氧化物水化物的溶液PH为12,氢氧根浓度为0.01mol/L,故为一元强碱,则X为Na,Y、W、Z对应的最高价氧化物水化物的溶液PH均小于7,均为酸,W最高价含氧酸溶液中氢离子浓度为0.01mol/L,故为一元强酸,则W为Cl元素;最高价含氧酸中,Z对应的酸性比W的强、Y对应的酸性比W的弱,而原子半径Y>Z>Cl,故Z为S元素,Y为P元素,据此解答.
解答:
解:第三周期元素中,X最高价氧化物水化物的溶液PH为12,氢氧根浓度为0.01mol/L,故为一元强碱,则X为Na,Y、W、Z对应的最高价氧化物水化物的溶液PH均小于7,均为酸,W最高价含氧酸溶液中氢离子浓度为0.01mol/L,故为一元强酸,则W为Cl元素;最高价含氧酸中,Z对应的酸性比W的强、Y对应的酸性比W的弱,而原子半径Y>Z>Cl,故Z为S元素,Y为P元素,
A.非金属性W>Z>Y,气态氢化物的稳定性:W>Z>Y,故A错误;
B.电子层结构相同,核电荷数越大离子半径越小,故离子半径S2->Cl-,故B错误;
C.Y为磷元素,单质有红磷、白磷,故C正确;
D.X和Y的最高价氧化物对应的水化物分别为NaOH、磷酸,恰好中和生成磷酸钠,溶液中磷酸根水解,溶液呈碱性,故D错误,
故选C.
A.非金属性W>Z>Y,气态氢化物的稳定性:W>Z>Y,故A错误;
B.电子层结构相同,核电荷数越大离子半径越小,故离子半径S2->Cl-,故B错误;
C.Y为磷元素,单质有红磷、白磷,故C正确;
D.X和Y的最高价氧化物对应的水化物分别为NaOH、磷酸,恰好中和生成磷酸钠,溶液中磷酸根水解,溶液呈碱性,故D错误,
故选C.
点评:本题考查结构性质位置关系应用,根据酸性、原子半径推断元素是解题关键,侧重对元素周期律的考查,难度中等.

练习册系列答案
相关题目
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、常温下28g乙烯中所含极性键的数目为4NA |
| B、将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NAFe3+ |
| C、标准状况下,22.4L甲醇的分子数中所含羟基数为NA |
| D、10L pH=1的硫酸溶液中含有的H+离子数为2NA |
设Na为阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol丙烯酸中含有双键的数目为Na |
| B、等质量14NO和13CO气体中含有的中子数相等 |
| C、一定量的钠与8g氧气作用,若两者均无剩余,转移Na个电子 |
| D、100mlpH=1的醋酸溶液中含有的氢离子数为0.01Na |
分类是化学学习与研究的常用方法,下列分类正确的是( )
| A、Cl2O7、P2O5、SO3、CO2均属于酸性氧化物 |
| B、盐酸、氢氧化钠、碳酸钾均为强电解质 |
| C、玻璃、水晶、陶瓷都是硅酸盐制品 |
| D、根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
下列物质的水溶液因水解呈酸性的是( )
| A、AlCl3 |
| B、Na2CO3 |
| C、NaCl |
| D、K2SO4 |
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述错误的是( )

| A、加入催化剂,不能改变该化学反应的反应热 |
| B、b曲线是加入催化剂时的能量变化曲线 |
| C、该反应的热化学方程式为:N2(g)+3H2(g)???2NH3(g),△H=-92 kJ/mol |
| D、在温度、体积一定的条件下,通入1 mol N2和3 molH2反应后放出的热量为92kJ |
有机物的结构可用“键线式”简化表示.如:CH3---CH═CH---CH3可以简写为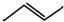 .有机物X的键线式为
.有机物X的键线式为 .下列说法不正确的是( )
.下列说法不正确的是( )
 .有机物X的键线式为
.有机物X的键线式为 .下列说法不正确的是( )
.下列说法不正确的是( )| A、X的化学式为C8H8 |
B、有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式: |
| C、X能使酸性高锰酸钾溶液褪色 |
| D、X与足量的H2在一定条件下反应可生成环状饱和烃Z,Z的一氯代物有4种 |
 丙烯酰胺是一种重要的有机合成的中间体.它的球棍模型如图所示:(图中球与球之间连线表示单键或双键,不同颜色球表示不同原子:C、H、O、N)
丙烯酰胺是一种重要的有机合成的中间体.它的球棍模型如图所示:(图中球与球之间连线表示单键或双键,不同颜色球表示不同原子:C、H、O、N)