题目内容
室温下,将1mol的CuSO4?5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2:CuSO4?5H2O受热分解的化学方程式为CuSO4?5H2O(s)
CuSO4(s)+5H2O(l),热效应为△H3,则下列判断正确的是( )
| ||
| A、△H2>△H3 |
| B、△H1<△H3 |
| C、△H1+△H3=△H2 |
| D、△H1+△H2>△H3 |
考点:用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:胆矾溶于水时,溶液温度降低,反应为CuSO4?5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H1>0;
CuSO4(s)=Cu2+(aq)+SO42-(aq)△H2;
已知CuSO4?5H2O(s)=CuSO4(s)+5H2O(l)△H3,根据盖斯定律确定之间的关系.
CuSO4(s)=Cu2+(aq)+SO42-(aq)△H2;
已知CuSO4?5H2O(s)=CuSO4(s)+5H2O(l)△H3,根据盖斯定律确定之间的关系.
解答:
解:①胆矾溶于水时,溶液温度降低,反应为CuSO4?5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H1>0;
②CuSO4(s)=Cu2+(aq)+SO42-(aq)△H2<0;
③已知CuSO4?5H2O(s)=CuSO4(s)+5H2O(l)△H3;
依据盖斯定律①-②得到③,所以△H3=△H1-△H2;△H2<0,△H1>0,则△H3>0,
A、上述分析可知△H2<△H3,故A错误;
B、分析可知△H2=△H1-△H3,由于△H2<0,△H3>△H1 ,故B正确;
C、△H3=△H1-△H2,故C错误;
D、△H2<0,△H1>0、△H3>△H1+△H2,故D错误;
故选B.
②CuSO4(s)=Cu2+(aq)+SO42-(aq)△H2<0;
③已知CuSO4?5H2O(s)=CuSO4(s)+5H2O(l)△H3;
依据盖斯定律①-②得到③,所以△H3=△H1-△H2;△H2<0,△H1>0,则△H3>0,
A、上述分析可知△H2<△H3,故A错误;
B、分析可知△H2=△H1-△H3,由于△H2<0,△H3>△H1 ,故B正确;
C、△H3=△H1-△H2,故C错误;
D、△H2<0,△H1>0、△H3>△H1+△H2,故D错误;
故选B.
点评:本题考查了物质溶解及物质分解过程中的能量变化,根据盖斯定律分析物质溶解过程中的能量变化是解题关键,题目难度中等.

练习册系列答案
相关题目
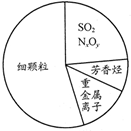 如图为雾霾的主要成分示意图.下列说法不正确的是( )
如图为雾霾的主要成分示意图.下列说法不正确的是( )| A、重金属离子可导致蛋白质变性 |
| B、苯是最简单的芳香烃 |
| C、SO2、NxOy都属于酸性氧化物 |
| D、利用丁达尔效应可检验雾霾是否为胶体 |
分子式为C9H12O,苯环上有两个取代基且含羟基的化合物,其可能的结构有( )
| A、9种 | B、12种 |
| C、15种 | D、16种 |
将a mol氢气和b mol乙烯混合,在一定条件下使它们部分反应生成c mol乙烷,将反应后的混合气体完全燃烧,消耗氧气的物质的量为( )
| A、(3b+0.5a)mol |
| B、(4b+0.5a)mol |
| C、(3b+1.5a)mol |
| D、无法判断 |