题目内容
10.下列实验装置或者操作正确的是 ( )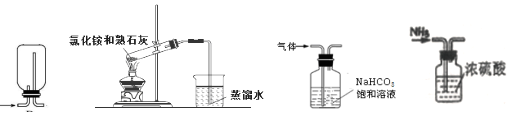
| A. | 排空气法收集氨气 | B. | 制氨水 | ||
| C. | 除二氧化碳中的少量二氧化硫 | D. | 干燥NH3 |
分析 A.氨气密度比空气小,应用向下排空法收集;
B.加热固体,应防止试管炸裂;
C.二氧化硫可与碳酸氢钠反应生成二氧化碳;
D.氨气与浓硫酸反应.
解答 解:A.氨气密度比空气小,应用向下排空法收集,则氨气应从长管进入,故A错误;
B.加热固体,试管口应略向下倾斜,以防止试管炸裂,故B错误;
C.二氧化碳不溶于饱和碳酸氢钠溶液,二氧化硫可与碳酸氢钠反应生成二氧化碳,可用于除杂,故C正确;
D.氨气与浓硫酸反应,不能用浓硫酸干燥,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、常见气体的制备、收集以及干燥原理为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.

练习册系列答案
相关题目
20.下列溶液中的溶质,不发生电离的是( )
| A. | 王水 | B. | 葡萄糖水 | C. | 食醋 | D. | 生理盐水 |
1.下列物质:①H3O+ ②[Cu(NH3)4]2+ ③CH3COO- ④NH3 ⑤CO中存在配位键的是( )
| A. | ①② | B. | ①②③ | C. | ③④⑤ | D. | ①②⑤ |
5.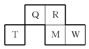 Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
 Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )| A. | MW6中各原子核外均满足8电子稳定结构 | |
| B. | Q、W的单核离子的核外电子数相等 | |
| C. | 五种元素均能形成氢化物 | |
| D. | W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强 |
3.A、B、C、D、E是五种元素,它们的核外电子排布如表所示:
(1)属于同一周期的元素是B、D、E(填元素符号,下同).
(2)属于同一主族的元素是A、C、E.
(3)B单质与水反应的化学反应方程式是2Na+2H2O=2NaOH+H2↑.
(4)E单质与水反应的化学反应方程式是Cl2+H2O=HCl+HClO.
| 元素 | 各电子层的电子数 | |||
| K | L | M | N | |
| A | 2 | 7 | ||
| B | 2 | 8 | 1 | |
| C | 2 | 8 | 18 | 7 |
| D | 2 | 8 | 2 | |
| E | 2 | 8 | 7 | |
(2)属于同一主族的元素是A、C、E.
(3)B单质与水反应的化学反应方程式是2Na+2H2O=2NaOH+H2↑.
(4)E单质与水反应的化学反应方程式是Cl2+H2O=HCl+HClO.
4.A、B、C为三种短周期元素,A、B在同周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构.下列说法中正确的是( )
| A. | 原子序数:A<B<C | B. | 原子半径:A>B>C | ||
| C. | 离子半径:A2->C->B2+ | D. | 原子核外最外层电子数:A>C>B |
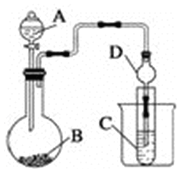 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.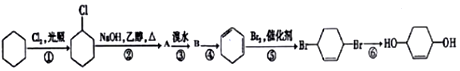
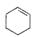 ,B的结构简式是
,B的结构简式是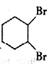 .
. .
.