题目内容
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.已知:A元素的原子半径最小;B与D同主族,D是一种很重要的半导体材料;C与E同主族,E元素原子的最外层电子数比次外层电子数少2.
(1)元素D在周期表中的位置是 .
(2)元素C的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物的电子式为 ,含有的化学键类型有 .
(3)F元素的最高价氧化物对应的水化物的电离方程式为 .
(4)由 C、D两种元素组成的化合物甲是工业制玻璃的原料之一,请写出甲与NaOH溶液反应的离子方程式 .
(5)E和F两种元素相比较,其原子得电子能力较强的是 (写名称).以下说法中,可以证明上述结论的是 (填写编号).
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,E元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氧化物的水化物的酸性.
(1)元素D在周期表中的位置是
(2)元素C的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物的电子式为
(3)F元素的最高价氧化物对应的水化物的电离方程式为
(4)由 C、D两种元素组成的化合物甲是工业制玻璃的原料之一,请写出甲与NaOH溶液反应的离子方程式
(5)E和F两种元素相比较,其原子得电子能力较强的是
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,E元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氧化物的水化物的酸性.
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,A元素的原子半径最小,则A为H元素;B与D同主族,D是一种很重要的半导体材料,则B为碳元素、D为Si;E元素原子的最外层电子数比次外层电子数少2,有3各个电子层、最外层电子数为6,故E为S元素;C与E同主族,则C为O元素;F的原子序数大于硫,故F为Cl,据此解答.
解答:
解:A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,A元素的原子半径最小,则A为H元素;B与D同主族,D是一种很重要的半导体材料,则B为碳元素、D为Si;E元素原子的最外层电子数比次外层电子数少2,有3各个电子层、最外层电子数为6,故E为S元素;C与E同主族,则C为O元素;F的原子序数大于硫,故F为Cl,
(1)元素D为Si,在周期表中的位置是:第三周期第ⅣA族,
故答案为:第三周期第ⅣA族;
(2)元素C的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物为Na2O2,其电子式为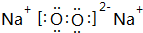 ,含有离子键、共价键,
,含有离子键、共价键,
故答案为: ;离子键、共价键;
;离子键、共价键;
(3)F元素的最高价氧化物对应的水化物为HClO4,属于强酸,其电离方程式为:HClO4═H++ClO4-,
故答案为:HClO4═H++ClO4-;
(4)由 O、Si两种元素组成的化合物甲为二氧化硅,二氧化硅与NaOH溶液反应的离子方程式为:SiO2+2OH-═SiO32-+H2O,
故答案为:SiO2+2OH-═SiO32-+H2O;
(5)E为S元素,F为Cl元素,同周期随原子序数增大,元素原子得电子能力增强,故氯原子得电子能力比硫的强,
a.单质的沸点属于物理性质,不能比较得电子能力,故a错误;
b.氯原子得电子能力强,与硫元素形成的化合物中S表现正价、氯表现负价,故b错误;
c.氢化物稳定性与非金属性一致,可以比较得电子能力,故c正确;
d.应比较最高价氧化物的水化物的酸性强弱,故d错误,
故答案为:氯原子;c.
(1)元素D为Si,在周期表中的位置是:第三周期第ⅣA族,
故答案为:第三周期第ⅣA族;
(2)元素C的单质与金属钠反应生成的化合物可作潜水面具中的供氧剂,这种化合物为Na2O2,其电子式为
 ,含有离子键、共价键,
,含有离子键、共价键,故答案为:
 ;离子键、共价键;
;离子键、共价键;(3)F元素的最高价氧化物对应的水化物为HClO4,属于强酸,其电离方程式为:HClO4═H++ClO4-,
故答案为:HClO4═H++ClO4-;
(4)由 O、Si两种元素组成的化合物甲为二氧化硅,二氧化硅与NaOH溶液反应的离子方程式为:SiO2+2OH-═SiO32-+H2O,
故答案为:SiO2+2OH-═SiO32-+H2O;
(5)E为S元素,F为Cl元素,同周期随原子序数增大,元素原子得电子能力增强,故氯原子得电子能力比硫的强,
a.单质的沸点属于物理性质,不能比较得电子能力,故a错误;
b.氯原子得电子能力强,与硫元素形成的化合物中S表现正价、氯表现负价,故b错误;
c.氢化物稳定性与非金属性一致,可以比较得电子能力,故c正确;
d.应比较最高价氧化物的水化物的酸性强弱,故d错误,
故答案为:氯原子;c.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意理解掌握金属性、非金属性比较实验事实.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化合物由碳、氢、氧三种元素组成,其红外光谱图只有C-H键,O-H键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式是( )
| A、CH3CH2OCH3 |
| B、CH3CH(OH)CH3 |
| C、CH3CH2OH |
| D、CH3COOH |
在25℃时,某溶液中由水电离出的c(H+)=1×10-12mol/L,则该溶液的pH可能是( )
| A、只有12 | B、只有2 |
| C、2或12 | D、6或7 |
 某温度时,在一个5L的体积不变的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个5L的体积不变的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题: X、Y、Z三种元素,原子序数依次减小.X是第四周期主族元素,其部分电离能如图所示;X、Y元素具有相同的最高正化合价;Z原子价电子排布式nsnnpn.回答下列问题:
X、Y、Z三种元素,原子序数依次减小.X是第四周期主族元素,其部分电离能如图所示;X、Y元素具有相同的最高正化合价;Z原子价电子排布式nsnnpn.回答下列问题: