题目内容
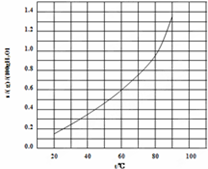
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )

| A、溴酸银的溶解是放热过程 |
| B、温度升高时溴酸银溶解速度加快 |
| C、60℃时溴酸银的KSP约等于6.25×10-4 |
| D、若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:A.无法判断其溶解过程的热效应;
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快;
C.60℃溴酸银的溶解度大约是0.6g.则c(AgBrO3)=
=0.025mol/L,Ksp=c(Ag+)?c(BrO3-)=0.025×0.025≈6×10-4;
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大.
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快;
C.60℃溴酸银的溶解度大约是0.6g.则c(AgBrO3)=
| 0.6g |
| 236g/mol×0.1L |
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大.
解答:
解:A.该图象只是给出溴酸银的溶解度与温度的关系,无法判断其溶解过程的热效应,故A错误;
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快,故B正确;
C.60℃溴酸银的溶解度大约是0.6g.则c(AgBrO3)=
=0.025mol/L,Ksp=c(Ag+)?c(BrO3-)=0.025×0.025≈6×10-4,故C正确;
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大,所以若硝酸钾中含有少量溴酸银,可用重结晶方法提纯,故D正确;
故选A.
B.温度升高,溴酸银溶解在水中的微粒运动速度加快,扩散的更快,故溶解速度加快,故B正确;
C.60℃溴酸银的溶解度大约是0.6g.则c(AgBrO3)=
| 0.6g |
| 236g/mol×0.1L |
D.由于硝酸钾的溶解度随温度变化比较大,而溴酸银的溶解度随温度变化不大,所以若硝酸钾中含有少量溴酸银,可用重结晶方法提纯,故D正确;
故选A.
点评:本题考查溶解度的概念及相关计算,难度中等.要注意重结晶方法的使用对象.

练习册系列答案
相关题目
下列关于容量瓶的说法不正确的是( )
| A、容量瓶上一般标有规格、温度和刻度线 |
| B、容量瓶在使用前要检查是否漏水 |
| C、可将固体或浓溶液直接在容量瓶中溶解或稀释 |
| D、容量瓶不能加热,也不宜长时间储存所配溶液 |
 可逆反应:mA(s)+nB(g)?qC(g)在一定温度的密闭容器中进行,B的体积分数(B%)与压强的关系如图所示.下列叙述正确的是( )
可逆反应:mA(s)+nB(g)?qC(g)在一定温度的密闭容器中进行,B的体积分数(B%)与压强的关系如图所示.下列叙述正确的是( )| A、m+n<q |
| B、n>q |
| C、n<q |
| D、x点时,v(正)<v(逆) |
将过量的氯气通入溴化钠溶液中,再向溶液中加入一定量的CCl4,充分振荡,观察到的现象是( )
| A、溶液有无色变橙色 |
| B、上层几乎无色,下层显橙色 |
| C、溶液由橙色变无色 |
| D、上层无色,下层为紫色 |
把下列物质的水溶液加热蒸干灼烧后,能得到原溶质的是( )
| A、NaHCO3 |
| B、FeCl3 |
| C、Mg (NO3)2 |
| D、Al2(SO4)3 |
在化学反应2H2O2═2H2O+O2中,H2O2中的氧元素( )
| A、只是被氧化 |
| B、只是被还原 |
| C、既被氧化又被还原 |
| D、以上都不是 |
VmL硫酸铁溶液中含wgSO42-,取此溶液0.5VmL,用水稀释成2VmL.则稀释后的溶液中Fe3+物质的量浓度为 (以下单位为mol?L-1)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
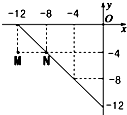 某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L.x与y的关系如图所示:
某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L.x与y的关系如图所示: