题目内容
3. 如图是M、N两种不含结晶水的固体物质溶解度曲线.下列说法中正确的是( )
如图是M、N两种不含结晶水的固体物质溶解度曲线.下列说法中正确的是( )| A. | t1℃时,N比M的溶解度大 | |
| B. | 温度从t1℃升高到t3℃时,N的饱和溶液张溶质的质量分数将增大 | |
| C. | M比N的溶解度大 | |
| D. | N中含有少量M时,可用降温结晶法提纯N |
分析 A.由图可知,t1℃时,N的溶解度大;
B.温度从t1℃升高到t3℃时,N的饱和溶液会析出固体N;
C.没有说明温度,无法比较;
D.降低温度N的溶解度会增大.
解答 解:A.由图可知,t1℃时,N对应的曲线在M的曲线的上方,所以N比M的溶解度大,故A正确;
B.温度从t1℃升高到t3℃时,N的溶解度减小,N的饱和溶液会析出固体N,所以N的饱和溶液的质量分数减小,故B错误;
C.没有说明温度,无法比较,t1℃时N的溶解度大,而t3℃时M的溶解度大,故C错误;
D.降低温度N的溶解度会增大,所以降低温度N不能析出固体,所以N中含有少量M时,不能用降温结晶法提纯N,故D错误.
故选A.
点评 本题考查了溶度积随温度的变化曲线,题目难度不大,注意把握图中曲线的含义以及影响溶解度大小的因素,侧重于考查学生的分析能力.

练习册系列答案
相关题目
13.下列叙述中正确的是( )
| A. | 过氧化钠是淡黄色固体,久置于空气中变成白色的氢氧化钠固体 | |
| B. | 过氧化钠中阴阳离子比例为1:2 | |
| C. | 用过氧化钠漂白织物、麦秆等日久又逐渐变成黄色 | |
| D. | Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 |
11.某溶液中含有Ba2+、Ag+、Cu2+三种离子,现用①NaOH溶液、②K2SO4溶液、③盐酸将这三种离子逐一沉淀并加以分离,则加入试剂顺序正确的是( )
| A. | ①②③ | B. | ③②① | C. | ②③① | D. | ②①③ |
1.某实验小组同学探究了铜与浓硫酸的反应,实验装置如图(1)所示.(夹持装置与A中加热装置已略,装置气密性已检验)

实验操作和现象:
(1)B溶液褪色,表明实验中产生的气体具有漂白性.
(2)三口瓶中的白色固体是CuSO4,验证你这一猜想的实验方案是取少量白色固体溶于水,溶液呈蓝色,说明固体中含有铜离子,向溶液中滴加氯化钡溶液并加入稀盐酸,出现白色沉淀,说明固体中含有硫酸根离子.
(3)A中产生该白色固体的化学方程式是2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(4)结束实验,拆除装置之前,为避免装置中的气体污染环境,应当采取的操作是向A中大量鼓入氮气或空气.
(5)A中产生的大量白雾,甲同学认为是硫酸沸腾后硫酸蒸气与水形成的酸雾.在不改变实验装置的情况下,甲同学设计实验初步证实其想法可能是正确的.甲同学的方案是将品红溶液换为盐酸酸化的氯化钡溶液,实验前先通入一段时间氮气,然后再加入装置A完成实验,若氯化钡溶液中出现白色沉淀,则甲的想法可能是正确的.
(6)有人认为实验过程中A中的黑色固体是CuO,乙同学认为不正确,其理由是CuO+H2SO4=CuSO4+H2O(用化学方程式表示).
(7)为研究A中黑色固体的成分,丙同学猜想其可能含有硫化铜或硫化亚铜.
查阅资料:硫化铜和硫化亚铜常温下均不溶于稀硫酸;在氧气气流中煅烧,均转化为氧化铜和二氧化硫.
丙同学收集到足够的黑色固体后,完成下列实验:

①黑色固体的成分及物质的量是CuS0.001mol、Cu2S0.005mol
②若A中黑色固体与浓硫酸反应能得到澄清的溶液,请写出该反应的化学方程式:5Cu2S+CuS+34H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$11CuSO4+29SO2↑+34H2O.

实验操作和现象:
| 实验序号 | 操作 | 现象 |
| 实验一 | 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中: (I)加热初期,Cu片表面变黑,溶液近乎无色 (II)继续加热,铜片表面产生气泡,形成黑色浊液,三口瓶底部有灰黑色固体沉积 (III)继续加热,有大量白雾生成,浊液变澄清,三口瓶底部有大量白色固体(因含有极少量黑色固体而显灰白色),Cu片消失B中有气泡冒出,溶液褪色 |
| 实验二 | 停止加热,冷却,将三口瓶中的上清液倒入盛有水的烧杯中 | 三口瓶中留有大量白色固体(因含有极少量黑色固体而显灰白色) 烧杯中溶液温度升高,溶液只略带蓝色 |
(2)三口瓶中的白色固体是CuSO4,验证你这一猜想的实验方案是取少量白色固体溶于水,溶液呈蓝色,说明固体中含有铜离子,向溶液中滴加氯化钡溶液并加入稀盐酸,出现白色沉淀,说明固体中含有硫酸根离子.
(3)A中产生该白色固体的化学方程式是2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(4)结束实验,拆除装置之前,为避免装置中的气体污染环境,应当采取的操作是向A中大量鼓入氮气或空气.
(5)A中产生的大量白雾,甲同学认为是硫酸沸腾后硫酸蒸气与水形成的酸雾.在不改变实验装置的情况下,甲同学设计实验初步证实其想法可能是正确的.甲同学的方案是将品红溶液换为盐酸酸化的氯化钡溶液,实验前先通入一段时间氮气,然后再加入装置A完成实验,若氯化钡溶液中出现白色沉淀,则甲的想法可能是正确的.
(6)有人认为实验过程中A中的黑色固体是CuO,乙同学认为不正确,其理由是CuO+H2SO4=CuSO4+H2O(用化学方程式表示).
(7)为研究A中黑色固体的成分,丙同学猜想其可能含有硫化铜或硫化亚铜.
查阅资料:硫化铜和硫化亚铜常温下均不溶于稀硫酸;在氧气气流中煅烧,均转化为氧化铜和二氧化硫.
丙同学收集到足够的黑色固体后,完成下列实验:

①黑色固体的成分及物质的量是CuS0.001mol、Cu2S0.005mol
②若A中黑色固体与浓硫酸反应能得到澄清的溶液,请写出该反应的化学方程式:5Cu2S+CuS+34H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$11CuSO4+29SO2↑+34H2O.
5.如表根据实验事实所作结论中,正确的是( )
| 实 验 事 实 | 结 论 | |
| A | A、B两种有机物具有相同的相对分子质量和不同的结构 | A、B互为同分异构体 |
| B | 质量相同的A、B两种有机物完全燃烧生成质量相同的水 | A、B两有机物最简式相同 |
| C | A、B两种有机物结构相似具有相同的通式 | A、B互为同系物 |
| D | 分子式为C6H6的烃A既能使溴的CCl4溶液褪色,又能使酸性KMnO4溶液褪色 | A的结构简式可能是 CH2═CH-C≡C-CH═CH2 |
| A. | A | B. | B | C. | C | D. | D |
6.用含有A12O3、SiO2和少量FeO•xFe2O3的铝灰制备A12(SO4)3•18H2O.工艺流程如图:

(一定条件下,MnO4-可与Mn2+反应生成MnO2)
已知:生成氢氧化物沉淀的pH
(1)H2SO4溶解A12O3的离子方程式是Al2O3+6H+=2Al3++3H2O;
(2)检验滤液中还存在Fe2+的方法是取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2;
(Ⅱ)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
(Ⅲ)加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的将Fe2+氧化为Fe3+;调节溶液的pH为3.2的目的是调节pH值使铁元素沉淀完全.
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是有黄绿色气体生成,写出其反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
③Ⅲ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式).

(一定条件下,MnO4-可与Mn2+反应生成MnO2)
已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
(2)检验滤液中还存在Fe2+的方法是取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2;
(Ⅱ)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
(Ⅲ)加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的将Fe2+氧化为Fe3+;调节溶液的pH为3.2的目的是调节pH值使铁元素沉淀完全.
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是有黄绿色气体生成,写出其反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
③Ⅲ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式).

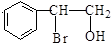 ,F分子中含有的含氧官能团名称是羟基、羧基(顺序可以颠倒).
,F分子中含有的含氧官能团名称是羟基、羧基(顺序可以颠倒). .
.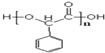 .
.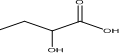 的合成线路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.
的合成线路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.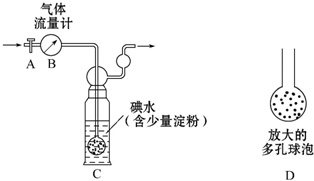 硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放.某化学研究性学习小组的同学欲采用以下方案测定硫酸工业尾气中SO2含量
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放.某化学研究性学习小组的同学欲采用以下方案测定硫酸工业尾气中SO2含量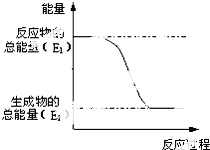 (1)“西气东输”中的“气”指天然气,其主要成分的化学式是CH4,
(1)“西气东输”中的“气”指天然气,其主要成分的化学式是CH4, .一定量的该气体燃烧过程的能量变化如图所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.
.一定量的该气体燃烧过程的能量变化如图所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.