题目内容
8.当光束通过下列物质时,不可能观察到丁达尔效应的是( )| A. | 稀豆浆 | B. | NaCl溶液 | C. | Fe(OH)3胶体 | D. | H2SiO3胶体 |
分析 依据分散系的分类和性质分析,胶体分散系具有丁达尔现象,只要判断出分散系是胶体即可.
解答 解:NaCl溶液属于溶液分散系,无丁达尔效应;豆浆、Fe(OH)3胶体、H2SiO3胶体分散质大小介于1nm~100nm,属于胶体,有丁达尔效应.
故选B.
点评 本题考查胶体的性质,丁达尔效应是胶体的特有性质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC.
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
写出B与稀H2SO4反应的离子方程式S2O32-+2H+=S↓+SO2↑+H2O,写出②中离子反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子),XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol.
(4)化合物D和E相互转化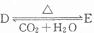 ,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC.
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子),XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol.
(4)化合物D和E相互转化
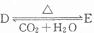 ,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
3.下列关于NH3性质的说法正确的是( )
| A. | 收集时采用向上排空气法 | B. | 能使湿润的红色石蕊试纸变蓝 | ||
| C. | 可用浓硫酸进行干燥 | D. | 不能与氧气反应 |
13.下列物质性质的比较中,不正确的是( )
| A. | 沸点:Br2>Cl2 | B. | 稳定性:HCl>HBr | ||
| C. | 酸性:H2SiO3>H2SO4 | D. | 碱性:Mg(OH)2<NaOH |
17.已知某溶液中存在较多的H+和SO42-,则该溶液中还可能大量存在的离子组是( )
| A. | Al3+、F-、Cl- | B. | K+、Cl-、CO32- | C. | HCO3-、Ba2+、I- | D. | Na+、NH4+、Cl- |
18.化学与生产、生活密切相关,下列有关说法不正确的是( )
| A. | 同位素的应用已经遍及医学、工业、农业、能源和科学研究的各个领域 | |
| B. | iPhone5外壳易掉色,是因为铝壳表面氧化处理过程中作为阴极的金属铝纯度不够,导致氧化膜不够致密 | |
| C. | 利用太阳能、风能和氢能等能源替代化石能源有利于实现“低碳经济” | |
| D. | 在医疗上硫酸亚铁可用于生产防治缺铁性贫血的药剂,在工业上硫酸亚铁还是生产铁系列净水剂的原料 |
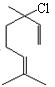 ;
;
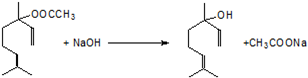 ,.
,. .
.