题目内容
下列化学用语表达正确的是( )
A、某离子结构示意图为: ,可以表示35Cl-,也可以表示37Cl- ,可以表示35Cl-,也可以表示37Cl- |
| B、X元素最高价氧化物对应的水化物为H2XO3,则它的气态氢化物为H2X |
C、二氧化碳分子的比例模型: |
| D、质子数为8,中子数为10的核素:10O |
考点:原子结构示意图,核素,球棍模型与比例模型
专题:化学用语专题
分析:A. 表示的是氯离子,可以表示所有的氯离子;
表示的是氯离子,可以表示所有的氯离子;
B.先根据X元素最高价氧化物对应的水化物为H2XO3,判断X的最外层电子数,再判断其氢化物分子式;
C.二氧化碳分子中,碳原子原子比较大于氧原子;
D.元素符号的左上角表示的是质量数,该核素的质量数为18.
 表示的是氯离子,可以表示所有的氯离子;
表示的是氯离子,可以表示所有的氯离子;B.先根据X元素最高价氧化物对应的水化物为H2XO3,判断X的最外层电子数,再判断其氢化物分子式;
C.二氧化碳分子中,碳原子原子比较大于氧原子;
D.元素符号的左上角表示的是质量数,该核素的质量数为18.
解答:
解:A. 的核电荷数为17,核外电子数为18,表示的是所有的氯离子,可以表示35Cl-,也可以表示37Cl-,故A正确;
的核电荷数为17,核外电子数为18,表示的是所有的氯离子,可以表示35Cl-,也可以表示37Cl-,故A正确;
B.X元素最高价氧化物对应的水化物为H2XO3,则X的最高正化合价为+4,最外层电子数为4,其氢化物的化学式为:H4X,故B错误;
C.二氧化碳为直线型结构,碳原子的原子半径大于氧原子,二氧化碳的比例模型为: ,故C错误;
,故C错误;
D.质子数为8,该元素为氧元素,中子数为10的核素,该氧原子的质量数为18,可以表示为:818O,故D错误;
故选A.
 的核电荷数为17,核外电子数为18,表示的是所有的氯离子,可以表示35Cl-,也可以表示37Cl-,故A正确;
的核电荷数为17,核外电子数为18,表示的是所有的氯离子,可以表示35Cl-,也可以表示37Cl-,故A正确;B.X元素最高价氧化物对应的水化物为H2XO3,则X的最高正化合价为+4,最外层电子数为4,其氢化物的化学式为:H4X,故B错误;
C.二氧化碳为直线型结构,碳原子的原子半径大于氧原子,二氧化碳的比例模型为:
 ,故C错误;
,故C错误;D.质子数为8,该元素为氧元素,中子数为10的核素,该氧原子的质量数为18,可以表示为:818O,故D错误;
故选A.
点评:本题考查了原子结构示意图、比例模型、元素符号及表示方法判断,题目难度中等,注意掌握常见的化学用语的表示方法,明确比例模型的概念及表示方法.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
下列属于电解质并能导电的物质是( )
| A、淀粉 |
| B、KNO3溶液 |
| C、FeCl3晶体 |
| D、熔融的NaCl |
苯的同系物C12H18有多种同分异构体,其中二取代苯的同分异构体(不考虑立体异构)有( )
| A、48种 | B、45种 |
| C、42种 | D、以上都不是 |
用惰性电极在一定温度下电解某Na2SO4饱和溶液,当两极共产生标准状况下67.2L气体时,从溶液中析出64.4g Na2SO4?10H2O 晶体.则剩余溶液的溶质质量分数约是( )
| A、64.7% |
| B、47.5% |
| C、32.2% |
| D、28.3% |
具有解热镇痛作用的阿斯匹林的结构式为: ,在适宜的条件下阿斯匹林可能发生的反应是
,在适宜的条件下阿斯匹林可能发生的反应是
①?消去反应;②?酯化反应;?③银镜反应;④?加成反应;?⑤水解反应;?⑥中和反应( )
 ,在适宜的条件下阿斯匹林可能发生的反应是
,在适宜的条件下阿斯匹林可能发生的反应是①?消去反应;②?酯化反应;?③银镜反应;④?加成反应;?⑤水解反应;?⑥中和反应( )
| A、????①②③④ |
| B、???①③⑤⑥ |
| C、???②③④⑤ |
| D、???②④⑤⑥ |
美国正在催日本归还超过300公斤的武器及放射物质,引发世界极大关注,
Pu中的中子数与质子数之差为( )
239 94 |
| A、239 | B、145 |
| C、94 | D、51 |
剧毒物质二恶英,其结构为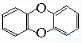 ,已知它的二氯代物有10种,则其六氯代物有( )
,已知它的二氯代物有10种,则其六氯代物有( )
 ,已知它的二氯代物有10种,则其六氯代物有( )
,已知它的二氯代物有10种,则其六氯代物有( )| A、15种 | B、11种 |
| C、10种 | D、5种 |