��Ŀ����
��14�֣�H2O2��һ�ֳ�����ɫ���������ڻ�ѧ�о���Ӧ�ù㷺��
��1����������������Ʊ�H2O2��װ������ͼ��ʾ����Ҫԭ�����ڼ��Ե������Һ�У�ͨ�����ÿ�����������������ԭ�õ�H2O2��ϡ��Ļ���
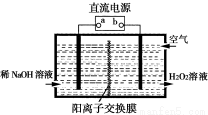
�Իش�
��ֱ����Դ��a�������� ��
�������缫��ӦʽΪ ��
��1979�꣬��ѧ������CO��O2��ˮ��������ٵĴ����Ƶ���H2O2������ڵ�ⷨ���÷������е��ŵ��ǰ�ȫ�� ��
��2��Fe3+��H2O2�ķֽ���д����á�����ͼ(a)��(b)�е���Ϣ����ͼ(c)װ�ã���ͨ��A��Bƿ���ѳ���NO2���壩����ʵ�顣�ɹ۲쵽Bƿ��������ɫ��Aƿ�е� ������dz��������ԭ���� ��
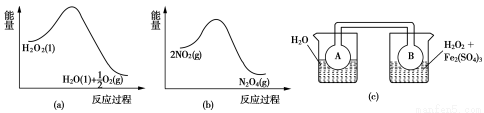
��3����H2O2 ��H2SO4 �Ļ����Һ���ܽ�ӡˢ��·�������ĩ�е�ͭ����Ӧ�����ӷ���ʽ�� ����������������ͬ��ӡˢ��·��Ľ�����ĩ��10%H2O2 ��3.0mol��L��1H2SO4��Һ��������ò�ͬ�¶���ͭ��ƽ���ܽ����ʣ����±���
�¶ȣ��棩 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
Cu��ƽ���ܽ����� ����10��3mol��min��1�� | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
���¶ȸ���40��ʱ��ͭ��ƽ���ܽ��������ŷ�Ӧ�¶ȵ����߶��½�������Ҫԭ���� ��
��1�������� �� O2 + 2e��+ 2H2O��H2O2 + 2OH�� ���ܺĵ�
��2������ ��H2O2�ֽ���ȣ�ʹƽ��2NO2 N2O4������NO2�����ƶ�
N2O4������NO2�����ƶ�
��3��Cu + H2O2 +2H+��Cu2+ + 2H2O���¶����ߣ�H2O2�ֽ����ʼӿ� ��ÿ��2�֣�
��������
�����������1���ٸ���װ��ͼ��֪�����Դb�������ĵ缫����˫��ˮ���������ÿ�����������������ԭ�õ�H2O2��ϡ��Ļ�����˵���õ缫����������b�Ǹ�������a��������
�ڵ����������õ����ӣ�������ԭ��Ӧ��˫��ˮ�������������������缫��ӦʽΪO2 + 2e��+ 2H2O��H2O2 + 2OH����
�����ڵ�ⷨ��Ҫ���Ĵ����ĵ��ܣ����Ը÷���������һ���ŵ����ܺĵ͡�
��2������Fe3+��H2O2�ķֽ���д����ã�����ͼ���֪��˫��ˮ�ֽ��Ƿ��ȷ�Ӧ������Bƿ����Һ�¶ȸߡ�����ΪNO2ת��ΪN2O3�Ƿ��ȷ�Ӧ�������¶ȴ�ʹƽ��2NO2 N2O4������NO2�����ƶ���������ɫ�
N2O4������NO2�����ƶ���������ɫ�
��3��˫��ˮ���������ԣ���ϡ������Һ���ܰ�ͭ������������ͭ��ˮ����Ӧ�����ӷ���ʽΪCu + H2O2 +2H+��Cu2+ + 2H2O������˫��ˮ���ȶ��������ֽ⣬�¶ȹ���ʱ����H2O2�ֽ����ʼӿ죬���ͭ��ƽ���ܽ��������ŷ�Ӧ�¶ȵ����߷����½���
���㣺����绯ѧԭ����Ӧ�á�˫��ˮ�����Լ���������Է�Ӧ���ʺ�ƽ��״̬��Ӱ��

 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д����и��������У�������������������������һ�������¾��ܷ�����Ӧ����
��� | �� | �� | �� |
A | Mg | FeSO4 | O2 |
B | Al2O3 | HCl | NaOH |
C | CO2 | H2O | Na2O2 |
D | NaHCO3 | Ca(OH)2 | Na2CO3 |
 2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ����v(H2)��������ƽ��ת���ʾ�����
2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ����v(H2)��������ƽ��ת���ʾ�����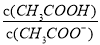 ��ֵ��С
��ֵ��С 2NaNO3(s)+2NO(g)+ Cl2(g)����H
2NaNO3(s)+2NO(g)+ Cl2(g)����H ����
���� Fe3O4��S4O62����2H2O������˵����ȷ����
Fe3O4��S4O62����2H2O������˵����ȷ����