题目内容
5.下列离子或分子组中,在相应的环境中一定能大量共存的是( )| 选项 | 环境要求 | 离子 |
| A | 溶液中c(K+)<c(Cl-) | K+、AlO2-、Cl-、NO3- |
| B | NaHCO3溶液 | K+、ClO-、AlO2- |
| C | 水电离产生的c(H+)=10-12 mol/L-1的溶液 | ClO-、CO32-、NH4+、NO3-、SO32- |
| D | 逐滴滴加氨水立即有沉淀产生 | Na+、HCO3-、Mg2+、SO42- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溶液中c(K+)<c(Cl-),由电荷守恒可知c(H+)>c(OH-),溶液应呈酸性;
B.与HCO3-反应的离子不能大量共存;
C.水电离产生的c(H+)=10-12 mol/L-1的溶液可能呈酸性或碱性;
D.逐滴滴加氨水立即有沉淀产生,应生成氢氧化镁,离子之间不发生反应.
解答 解:A.溶液中c(K+)<c(Cl-),由电荷守恒可知c(H+)>c(OH-),溶液应呈酸性,酸性条件下AlO2-不能大量共存,故A错误;
B.AlO2-与HCO3-发生互促水解反应而不能大量共存,故B错误;
C.水电离产生的c(H+)=10-12 mol/L-1的溶液可能呈酸性或碱性,碱性条件下NH4+不能大量共存,酸性条件下ClO-、NO3-与SO32-发生氧化还原反应而不能大量共存,故C错误;
D.逐滴滴加氨水立即有沉淀产生,应生成碳酸镁,离子之间不发生反应,可大量共存,故D正确.
故选D.
点评 本题考查离子共存,为高考常见题型,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,注意把握离子的性质以及反应类型的判断,把握题给信息,难度中等.

练习册系列答案
相关题目
15.己知A、B、C、D的原子序数都不超过18,它们的离子aA(n+l)+、bBn+、.cC(n+l)-、dDn-均具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子序数:a>b>c>d | B. | 离子半径:C(n+1)->Dn->A(n+1)+>Bn+ | ||
| C. | 单质还原性:B>A,氧化性:D>C | D. | 原子半径:A>B>C>D |
16. CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
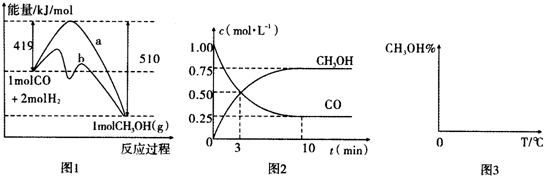
(1)用甲烷与水蒸气制备合成气,每生成1mol合成气,需要供给51.5kJ热量.该反应的热化学方程式为CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206KJ/mol.
(2)在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g).测得CH4和H2的物质的量浓度随时间变化如下表所示:
①该反应第一次达平衡时的平衡常数K=0.135.
②3min时改变的反应条件是升高温度或增大H2O(g)的浓度或减小CO的浓度(只填一种条件的改变即可).
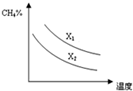
(3)已知一定压强下,温度、投料比X[$\frac{n(C{H}_{4})}{n({H}_{2}O)}$]对该反应的影响如图所示.图中的两条曲线所示投料比的关系X1>X2(填“=”、“>”或“<”).
 CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.(1)用甲烷与水蒸气制备合成气,每生成1mol合成气,需要供给51.5kJ热量.该反应的热化学方程式为CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206KJ/mol.
(2)在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g).测得CH4和H2的物质的量浓度随时间变化如下表所示:
| 浓度(mol/L) 物质 时间/min | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2 | 0.13 | 0.1 | 0.1 | 0.09 |
| H2 | 0 | 0.21 | 0.3 | 0.3 | 0.33 |
②3min时改变的反应条件是升高温度或增大H2O(g)的浓度或减小CO的浓度(只填一种条件的改变即可).
(3)已知一定压强下,温度、投料比X[$\frac{n(C{H}_{4})}{n({H}_{2}O)}$]对该反应的影响如图所示.图中的两条曲线所示投料比的关系X1>X2(填“=”、“>”或“<”).
20.一定条件下,可逆反应的平衡常数可以用平衡浓度计算.也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数.在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便.下列说法不正确的是( )
| A. | 对于C2H4(g)+H2O(g)═C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为l mol,则用分压表示的平衡常数Kp=$\frac{3}{P}$ | |
| B. | 恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)═2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol.若此时A、B和C均增加1 mol,平衡正向移动 | |
| C. | 一恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)═2NH3(g)达到平衡状态时,N2、H2、NH3各l mol,若此时再充入3mol N2,则平衡正向移动 | |
| D. | 对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关 |
10.短周期元素A、B可形成A3B2型化合物,若B的原子序数为 b,则A的原子序数不可能为( )
| A. | b-3 | B. | b+5 | C. | b+4 | D. | b一11 |
14.短周期主族元素W、X、Y、Z的原子序数依次增大.W、Z同族,Y、Z相邻,W、Y、Z三种元素原子的最外层电子数之和为11,X原子最外层电子数等于最内层电子数的一半.下列叙述正确的是( )
| A. | 金属性:X<Y | |
| B. | 原子半径:Y>Z | |
| C. | 最简单氢化物的热稳定性:Z>W | |
| D. | Y元素氧化物不溶于X元素最高价氧化物对应水化物的水溶液 |
15.在如图装置中,铁片上没有气泡产生的是( )
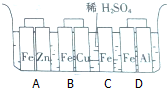

| A. | A | B. | B | C. | C | D. | D |
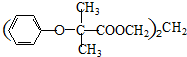
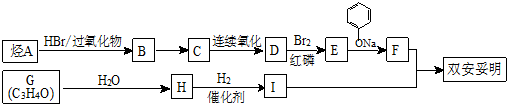
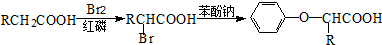
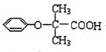 .
.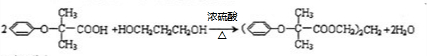 .
. .
.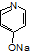 (
(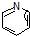 与
与 苯环性质相似)与
苯环性质相似)与 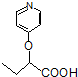 合成的路线:
合成的路线: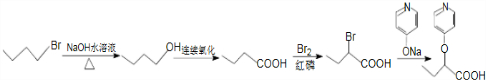 .
.