题目内容
11.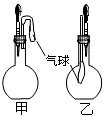 甲、乙两个装置中(如图),胶头滴管分别吸有某液体,平底烧瓶中置有其他物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).所用试剂分别是( )
甲、乙两个装置中(如图),胶头滴管分别吸有某液体,平底烧瓶中置有其他物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).所用试剂分别是( )| A. | 甲:浓硫酸和木炭 乙:浓氨水和SO2 | |
| B. | 甲:双氧水和MnO2 乙:NaOH溶液和CO2 | |
| C. | 甲:苯酚和Na2CO3溶液 乙:NaOH溶液和Cl2 | |
| D. | 甲:浓硫酸和蔗糖(滴有几滴水) 乙:水和氨气 |
分析 由图可知,甲装置中的气球明显胀大,说明反应生成较多的气体,内部压强大于外压;而乙装置中的气球明显胀大,说明反应导致内部气体减少,外压大于内压,然后结合物质的性质及发生的反应来解答.
解答 解:A.浓硫酸和木炭常温下不反应,甲中气球不变,而浓氨水和SO2反应导致气体减少,则乙中气球变大,故A不选;
B.双氧水和MnO2反应生成氧气,甲中气球变大,且NaOH溶液和CO2反应导致气体减少,则乙中气球变大,故B选;
C.苯酚和Na2CO3溶液反应不生成气体,甲中气球不变,而NaOH溶液和Cl2反应导致气体减少,则乙中气球变大,故C不选;
D.甲中浓硫酸稀释放出大量的热,且具有强的氧化性和吸水性,能够使蔗糖碳化且发生氧化还原反应生成二氧化碳、二氧化硫,烧瓶内气体增加,压强增大,气体胀大,且乙中氨气溶于水,使烧瓶内气体体积减小,压强减小,气球胀大,故D选;
故选BD.
点评 本题考查实验装置的综合应用及元素化合物知识,为高频考点,把握物质的性质和气球膨胀的原理是解题关键,侧重分析与应用能力的综合考查,题目难度不大.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
1.有M、N、P、Q四块金属片,进行如下实验:
①M、N用导线相连后,同时插入稀H2SO4中,M极为负极
②P、Q用导线相连后,同时浸入稀H2SO4中,电子由P→导线→Q
③M、P相连后,同时浸入稀H2SO4,P极产生大量气泡
④N、Q相连后,同时浸入稀H2SO4中,Q极发生氧化反应
由此判断四种金属的活动性顺序为( )
①M、N用导线相连后,同时插入稀H2SO4中,M极为负极
②P、Q用导线相连后,同时浸入稀H2SO4中,电子由P→导线→Q
③M、P相连后,同时浸入稀H2SO4,P极产生大量气泡
④N、Q相连后,同时浸入稀H2SO4中,Q极发生氧化反应
由此判断四种金属的活动性顺序为( )
| A. | M>P>Q>N | B. | P>M>N>Q | C. | N>Q>P>M | D. | M>N>P>Q |
19.党的十八大报告中提出“大力推进生态文明建设,提高生态文明水平,建设美丽中国”.为了实现这一目标,从化学的角度分析,下列说法正确的是( )
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
6.为除去试样中括号内的杂质,选用的试剂正确的是( )
| A | B | C | D | |
| 试样 | Na2CO3(NaHCO3) | CO2(HCl) | FeCl2(FeCl3) | CO2(SO2) |
| 除杂试剂 | 澄清石灰水 | 饱和Na2CO3溶液 | 铁粉 | 饱和NaHSO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
16.关于物质的检验,下列判断正确的是( )
| A. | 在溶液中加入盐酸酸化,无现象;再加入BaCl2溶液,如果生成白色沉淀,则原溶液中一定有大量的SO42-存在 | |
| B. | 在溶液中加入AgNO3溶液,生成不溶于硝酸的沉淀,则原溶液中一定有Cl-存在 | |
| C. | 在溶液中加入浓NaOH溶液,加热后如果生成气体使湿润的红色石蕊试纸变蓝,则原溶液一定是铵盐溶液 | |
| D. | 在溶液中加入KSCN溶液,无现象;再加入稀硝酸,溶液变血红色,则原溶液中一定有Fe2+存在 |
3.炼钢时,将氧气、生石灰加入熔融生铁后,会发生多个反应,其中不可能生成的是( )
| A. | CaSiO3 | B. | Ca3(PO4)2 | C. | Fe2O3 | D. | CO |
20.已知25℃时H2SO3 和H2CO3的电离平衡常数(电离平衡常数越大,酸的电离程度越大),有关 ①100mL 0.1mol/L NaHCO3、②100mL 0.1mol/LNaHSO3两种溶液的叙述正确的是( )
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-4 |
| H2CO3 | 4.4×10-7 | 4.7×10-11 |
| A. | 溶液中水电离出的OHˉ个数:①<② | |
| B. | 溶液中分子的微粒数:H2SO3<H2CO3 | |
| C. | 溶液①中:c(Na+)>c(HCO3-)>c(OHˉ)>c(CO32-)>c(H+) | |
| D. | 溶液②中:c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OHˉ) |
14.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1mol/L BaCl2溶液中含Cl-数目为0.2NA | |
| B. | 2.8gN2和CO的混合气体中含原子数目0.2NA | |
| C. | 5.6gFe在足量氯气中燃烧,转移电子数目0.2NA | |
| D. | 标况下2.24LCH3COOH中含碳原子数目为0.2NA |
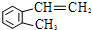 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.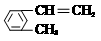 .
.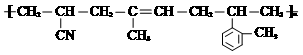 (假设按1:1:1的单体比例合成).
(假设按1:1:1的单体比例合成).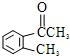 ,写出相关的化学方程式:
,写出相关的化学方程式: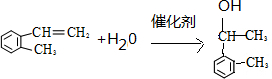 、
、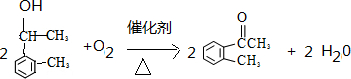 .
.