题目内容
3.下列说法正确的是( )| A. | 常温下可用铁制或铝制容器盛装浓硝酸 | |
| B. | 高炉炼铁的主要反应原理是碳在高温下直接将氧化铁还原成铁 | |
| C. | SO2气体可使酸性高锰酸钾溶液褪色,体现了SO2的漂白性 | |
| D. | 二氧化碳和二氧化硅都是酸性氧化物,都能与水反应生成相应的酸 |
分析 A、铁与铝与冷的浓硝酸发生钝化现象;
B、高炉炼铁的主要反应原理是CO在高温下直接将氧化铁还原成铁;
C、二氧化硫与酸性高锰酸钾发生氧化还原反应;
D、二氧化硅与水不反应.
解答 解:A、铁与铝与冷的浓硝酸发生钝化现象,所以日常生活中用铁或铝制容器盛装浓硝酸,故A正确;
B、高温下,碳被氧化二氧化碳,二氧化碳和C反应生成CO,所以高炉炼铁的主要反应原理是CO在高温下直接将氧化铁还原成铁,故B错误;
C、二氧化硫与酸性高锰酸钾发生氧化还原反应,二氧化硫的还原性,而不是漂白性,故C错误;
D、二氧化硅与水不反应,不能生成相应的酸,故D错误.
故选A.
点评 本题主要考查二氧化硅、二氧化硫和浓硝酸的性质、组成以及用途,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
13.下列措施或事实不能用勒沙特列原理解释的是( )
| A. | 滴加酚酞的氨水中加入氯化铵固体后红色变浅 | |
| B. | 棕红色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)?N2O4 (g)) | |
| C. | 工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 | |
| D. | 用硫酸氢钠去除暖水瓶中的水垢 |
14.下列变化过程中,没有发生化学变化的是( )
| A. | 铁的钝化 | B. | 光合作用 | C. | 碘的升华 | D. | 燃放烟花 |
11.下列离子方程式正确的是( )
| A. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| C. | 碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-═H2O+CO2↑ | |
| D. | 将氯气通入KBr溶液中:Cl2+2Br-═2Cl-+Br2 |
18.下列关于证明醋酸是弱电解质的实验方法不正确的是( )
| A. | 常温下,测定0.1mol•L-1CH3COOH的pH值,若pH大于1,即可证明为弱电解质 | |
| B. | 等体积的0.1mol•L-1HCl和0.1mol•L-1醋酸溶液,分别与等量的相同颗粒度的Zn反应,观察产生气泡的速率,即可证明 | |
| C. | 等体积的0.1mol•L-1HCl和 0.1mol•L-1醋酸溶液,比较中和这两种酸所需相同物质的量浓度的NaOH溶液的体积,即可证明 | |
| D. | 常温下,测一定浓度的CH3COONa溶液的pH值,若pH大于7,即可证明 |
8.下列说法不正确的是( )
| A. | 用元素分析仪来确定有机化合物的组成具有快速、微量、精确等特点 | |
| B. | 根据1H核磁共振谱图可以推知有机物分子中有几种不同类型的氢原子 | |
| C. | 用铜丝燃烧法可定性确定有机物中是否存在卤素 | |
| D. | 通过红外光谱可以测知有机物的相对分子质量 |
17.下列说法正确的是( )
| A. | 化合物 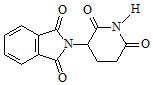 的分子式为C13H9O4N2 的分子式为C13H9O4N2 | |
| B. | CH3(CH2)2CH3与CH(CH3)3具有不同数目的一氯代物 | |
| C. | 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应 | |
| D. | 石油的裂化、裂解属于化学变化,煤的气化、液化则属于物理变化 |
18.在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,下列电解质中不适宜加入的是( )
| A. | KNO3 | B. | KI | C. | H2SO4 | D. | Ba(OH)2 |