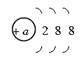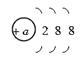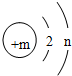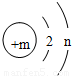题目内容
某粒子的结构示意图如图所示,试回答: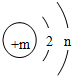
(1)当m-n=2时,该粒子为
(2)当n=8且m>n+2时,该粒子可能是(写离子符号):
(3)写出n=4与n=6的两元素所形成的化合物的化学式
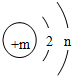
(1)当m-n=2时,该粒子为
原子
原子
(填“原子”、“阳离子”或“阴离子”)(2)当n=8且m>n+2时,该粒子可能是(写离子符号):
Na+
Na+
、Mg2+
Mg2+
、Al3+
Al3+
.(3)写出n=4与n=6的两元素所形成的化合物的化学式
CO、CO2
CO、CO2
.分析:(1)根据微粒的质子数和核外电子排布知识来回答.
(2)根据10电子微粒知识来回答;
(3)根据原子核外电子排布知识,确定n=4与n=6的两元素,进而确定形成的化合物.
(2)根据10电子微粒知识来回答;
(3)根据原子核外电子排布知识,确定n=4与n=6的两元素,进而确定形成的化合物.
解答:解:(1)当m-n=2时,质子数等于2+最外层电子数,所以是原子,故答案为:原子;
(2)当n=8且m>n+2时,该粒子可能是钠离子、镁离子、铝离子,故答案为:Na+;Mg2+;Al3+;
(3)当n=4时,元素为C,n=6时,元素为O,两元素所形成的化合物为CO、CO2,故答案为:CO、CO2.
(2)当n=8且m>n+2时,该粒子可能是钠离子、镁离子、铝离子,故答案为:Na+;Mg2+;Al3+;
(3)当n=4时,元素为C,n=6时,元素为O,两元素所形成的化合物为CO、CO2,故答案为:CO、CO2.
点评:本题考查学生原子核外电子排布知识,可以根据所学知识来回答,难度不大.

练习册系列答案
相关题目