题目内容
10.设NA为阿伏加德罗常数,常压下CH4在一定量O2中燃烧.下列说法正确的是( )| A. | 120℃时,若反应前混合气体共NA个分子,反应后气体分子可能大于NA | |
| B. | 0℃时,若生成2.24L气体,则转移电子数一定为0.8NA | |
| C. | 若NA个CH4分子参加反应,则有 2NA个O-H生成 | |
| D. | 0℃时,若NA个CH4分子和足量O2完全反应,则生成气体体积为67.2L |
分析 A.①当氧气不充足时,在120℃时,甲烷和氧气发生的反应为CH4(g)+O2(g)→CO(g)+2H2O(g),这是一个气体体积增大的反应,应前混合气体共NA个分子,则反应后气体分子大于NA,②当氧气充足时,在120℃时,甲烷和氧气发生的反应为CH4(g)+2O2(g)→CO2(g)+2H2O(g),这是一个气体体积不变的反应,应前混合气体共NA个分子,则反应后气体分子等于于NA,据此进行分析;
B.0℃时,若氧气不充足时,甲烷和氧气发生的反应为CH4(g)+O2(g)→CO(g)+2H2O(l),n(CO)=$\frac{2.24L}{22.4L/mol}$=0.1mol,
CH4(g)+O2(g)→CO(g)+2H2O(l)~6mole-
1 6
0.1 0.6,据此进行分析;
C.根据元素守恒分析;
D.0℃时,甲烷和足量的氧气发生的反应为CH4(g)+2O2(g)→CO2(g)+2H2O(l),
CH4(g)+2O2(g)→CO2(g)+2H2O(l)
NA 22.4,故生成气体22.4L,据此进行分析;
解答 解:A.①当氧气不充足时,在120℃时,甲烷和氧气发生的反应为CH4(g)+O2(g)→CO(g)+2H2O(g),这是一个气体体积增大的反应,反应前混合气体共NA个分子,则反应后气体分子大于NA,②当氧气充足时,在120℃时,甲烷和氧气发生的反应为CH4(g)+2O2(g)→CO2(g)+2H2O(g),这是一个气体体积不变的反应,应前混合气体共NA个分子,则反应后气体分子等于于NA,故反应后气体分子可能大于NA,故A正确;
B.0℃时,若氧气不充足时,甲烷和氧气发生的反应为CH4(g)+O2(g)→CO(g)+2H2O(l),n(CO)=$\frac{2.24L}{22.4L/mol}$=0.1mol,
CH4(g)+O2(g)→CO(g)+2H2O(l)~6mole-
1 6
0.1 0.6,故转移电子数一定为0.6NA,故B错误;
C.NA个CH4分子中含H原子个数为4NA个,根据H元素守恒,则生成2NA个H2O,1个H2O中含有2个O-H,故2NA个H2O中含有4NA个O-H,故C错误;
D.0℃时,甲烷和足量的氧气发生的反应为CH4(g)+2O2(g)→CO2(g)+2H2O(l),
CH4(g)+2O2(g)→CO2(g)+2H2O(l)
NA 22.4,故生成气体22.4L,故D错误,
故选A.
点评 本题考查阿伏加德罗常数的有关计算,题目难度稍大,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意合理分析甲烷与氧气的反映情况,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案| A. | H、D、T互为同素异形体 | |
| B. | H2O2分子中含有非极性键和极性共价键 | |
| C. | NH4Cl的电子式为: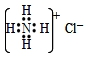 | |
| D. | CO2分子的比例模型图: |
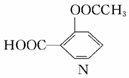
| A. | 分子式是C9H8O4 | |
| B. | 属于酯类化合物 | |
| C. | 1 molN 可以与1 mo1Na2CO3充分反应生成lmolCO2 | |
| D. | 一定条件下可发生加成反应和取代反应 |
| A. | 200g 63%的浓硝酸中含氧原子的数目为6NA | |
| B. | 已知C2H4(g)+H2(g)═C2H6(g)△H=-137.0kJ/mol,乙稀与H2加成时放出68.5kJ热量,则反应过程中被破坏的碳原子之间的共用电子对数目为NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标况下)气体时,电路中通过的电子数目为2NA | |
| D. | 若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的数目大于6NA |
| A. | Fe3+、K+、OH-、Cl- | B. | Na+、Zn2+、CO32-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ba2+、CO32-、NO3-、K+ |
| A. | Na2O2中阴、阳离子个数比为1:1 | |
| B. | Na2O2分别与水及CO2反应产生相同量O2时,需水和CO2的质量相等 | |
| C. | Na2O2与SO2的漂白原理相同 | |
| D. | 与H2O、CO2反应产生等量O2时,消耗等量的Na2O2 |
| A. | 蒸发皿加热时均需要垫上石棉网 | |
| B. | 分液漏斗使用前均需要检查是否漏水 | |
| C. | 配制1 mol•L-1NaCl溶液、测定Na2CO3溶液的pH、焰色反应实验均需要用到玻璃棒 | |
| D. | 氯水存放在配有磨口塞的广口瓶中 |
 :甲的化学式为Si3N4.
:甲的化学式为Si3N4.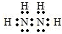 .
.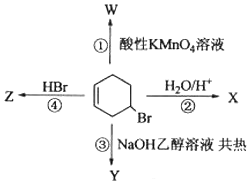
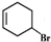 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$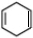 +NaBr+H2O
+NaBr+H2O