题目内容
(5分)某大理石含有的主要杂质是氧化铁,以下是提纯该大理石的实验步骤:
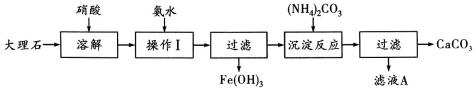
(1)溶解大理石时,用硝酸而不用硫酸的原理是: 。
(2)操作Ⅰ的目的是: ,该反应的离子方程式是: 。
(3)写出加入(NH4)2CO3所发生反应的离子方程式: ,
滤液A的一种用途是 。
(1) 硫酸钙微溶于水。
(2) 除Fe3+离子;Fe3++3NH3·H2O = Fe(OH)3↓+3NH4+
(3) Ca2++CO32- = CaCO3↓,做化肥。
【解析】
试题分析:溶解大理石时,用硝酸而不用硫酸的原理是因为硫酸钙微溶于水,如果用硫酸则不会使碳酸钙完全溶解;加氨水的目的是除去杂质Fe3+,离子方程式为: Fe3++3NH3·H2O = Fe(OH)3↓+3NH4+;加入(NH4)2CO3目的是使Ca2+沉淀Ca2++CO32- = CaCO3↓,滤液A的主要成分是NH4NO3可做氮肥。
考点:工艺流程推断。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目