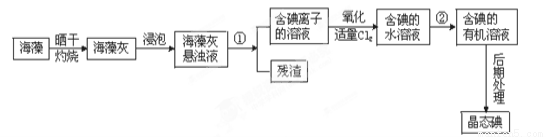
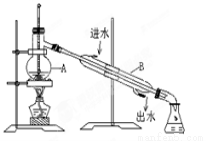
题目内容
(12分)(1)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-) / c(H+)=1×10-8。
①常温下,0.1 mol·L-1 HA溶液的pH= ;写出该酸(HA)与NaOH溶液反应的离子方程式: ;
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是: 。
(2)常温下,向pH=a的氨水中加入等体积盐酸时,溶液呈中性,则此盐酸的pH 14-a(>、<、=)
(3)向物质的量浓度均为0.01 mol·L-1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的离子是 ,当两种难溶电解质共存时,溶液中c(Ba2+)/c(Mn2+)= 。(此温度下,Ksp(BaCO3)=8.1×10-9、Ksp(MnCO3)=1.8×10-11)
(1)① 3 , HA+OH-=A-+H2O
②c (A-)> c (Na+)> c (H+)> c (OH-)
(2)<
(3)Mn2+, 450
【解析】
试题分析:(1)①根据c(OH-) / c(H+)=1×10-8 ,c(OH-) ×c(H+)=1×10-14 可知溶液中
c(H+)=1×10-3mol/L,pH=3;该酸为弱酸,与NaOH溶液反应的离子方程式为HA+OH-=A-+H2O
②pH=11的NaOH溶液中c(OH-)=10-3mol·L-1,HA是弱酸,酸的浓度远远大于氢离子浓度,所以pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中的溶质是酸和盐,溶液呈酸性,所以溶液中氢离子浓度大于氢氧根离子浓度,酸根离子浓度大于钠离子浓度,溶液中4种离子物质的量浓度大小关系是
c(A-)>c(Na+)>c(H+)>c(OH-),
(2) 假设氨水是强电解质时,pH=a的氨水中氢氧根离子浓度=10a-14mol·L-1,向pH=a的氨水中加入等体积盐酸时,溶液呈中性,则氢氧根离子浓度等于氢离子浓度,所以盐酸的pH=14-a;实际上氨水是弱碱,等体积的酸和碱混合后溶液呈中性,说明酸的浓度大于碱的浓度,则盐酸的pH<14-a,故选<。
(3) 碳酸钡的溶度积常数等于碳酸锰的溶度积常数,所以锰离子先沉淀;当两种难溶电解质共存时,则c(CO32-)=c(Mn2+)=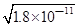 ,溶液中c(Ba2+)=
,溶液中c(Ba2+)= ,
,
c(Ba2+):c(Mn2+)= /
/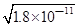 =450,故答案为:Mn2+;450 。
=450,故答案为:Mn2+;450 。
考点:弱电解质的电离、溶液的pH、难溶电解质的KSP

 一线名师权威作业本系列答案
一线名师权威作业本系列答案食物是维持人类生命和健康的支柱。下表是某食品包装袋上的说明:
品名 | 蔬菜苏打饼 |
配料 | 面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁 |
保质期 | 十二个月 |
生产日期 | 2008年11月6日 |
对上表中各种配料成分的理解不正确的是
A.富含蛋白质的是鲜鸡蛋
B.富含维生素的是脱水青菜和橙汁
C.富含淀粉的是面粉和白砂糖
D.富含油脂的是精炼食用植物油和奶油
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从表格中判断以下说法中不正确的是
A.在冰醋酸中这四种酸都没有完全电离
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中硫酸的电离方程式为H2SO4=2H++ SO42-
D.水对于这四种酸的强弱没有区分能力,但在醋酸中可以区别这四种酸的强弱
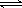 2SO3(g),下列判断不正确的是
2SO3(g),下列判断不正确的是 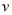 正(O2)=
正(O2)=