题目内容
8.标准状况下,下列关于气体的说法中正确的是( )| A. | 2mol氧气与1mol二氧化硫的质量比约为2:1 | |
| B. | 2mol氧气与1mol二氧化硫的体积比约为1:1 | |
| C. | 1mol氧气与3mol二氧化硫的体积比约为1:3 | |
| D. | 1mol氧气与3mol二氧化硫的密度比约为1:3 |
分析 A.依据m=NM计算解答;
B.依据V=nVm解答;
C.依据V=nVm解答;
D.依据ρ标=$\frac{M}{Vm}$解答.
解答 解:A.2mol氧气与1mol二氧化硫的质量比约为2mol×32g/mol:1mol×64g/mol=1:1,故A错误;
B.依据V=nVm,相同状况下气体体积之比等于物质的量之比,所以2mol氧气与1mol二氧化硫的体积比约为2:1,故B错误;
C.依据V=nVm,相同状况下气体体积之比等于物质的量之比,所以1mol氧气与3mol二氧化硫的体积比约为1:3,故C正确;
D.依据ρ标=$\frac{M}{Vm}$可知,气体的密度之比等于其摩尔质量之比,所以1mol氧气与3mol二氧化硫的密度比约为:32:64=1:2,故D错误;
故选:C.
点评 本题考查了物质的量的有关计算,明确物质的量与分子数的关系及分子构成是解本题关键,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
18.化学反应SO2+NO2=SO3+NO的反应类型是( )
| A. | 化合反应 | B. | 氧化还原反应 | C. | 置换反应 | D. | 复分解反应 |
19.下列有关物质检验的实验结论正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液溶液变红 | Fe(NO3)2样品已氧化变质 |
| C | 向盛有少量NaHCO3的试管中滴加草酸溶液有气泡产生 | 酸性:草酸>碳酸 |
| D | 向少量某物质的稀溶液中滴加稀盐酸,产生了能使澄清石灰水变浑浊的气体 | 该物质一定是碳酸盐 |
| A. | A | B. | B | C. | C | D. | D |
16.H、C、N、O、Na、Al、S、Cl、Ca是常见的9种元素.
(1)写出由上述9种元素的几种组成的既含有离子键又含共价键的离子化合物的化学式NaOH(或NaClO、Na2O2等);既含极性共价键又含非极性共价键的共价化合物的化学式H2O2(或C2H4、N2H4).
(2)O元素的一种中子数为10的核素的符号表示为818O,N的原子结构示意图 .
.
(3)上述9种元素中的金属工业冶炼方法是A
A.全部采用电解法
B.其中2种采用电解法,另外一种采用热分解法
C.其中一种采用电解法,另外两种采用热还原法
D.全部采用加热分解法
(4)用“大于”“小于”或“等于”填空
(5)甲与乙在溶液中的转化关系如右图所示(反应条件省略)甲不可能是D.
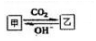
A.NH3 B.AlO2- C.CO32- D.CH3COO-
(6)CaCO3和适量HCl溶液反应,当反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得PH变化曲线如图所示.
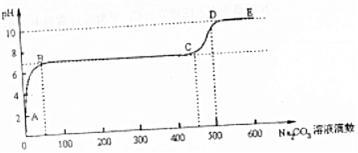
请用离子方程式表示B-C段发生的反应Ca2++CO32-=CaCO3↓;C点到D点pH增大的原因可用离子方程式表示为CO32-+H2O?HCO3-+OH-.
(1)写出由上述9种元素的几种组成的既含有离子键又含共价键的离子化合物的化学式NaOH(或NaClO、Na2O2等);既含极性共价键又含非极性共价键的共价化合物的化学式H2O2(或C2H4、N2H4).
(2)O元素的一种中子数为10的核素的符号表示为818O,N的原子结构示意图
 .
.(3)上述9种元素中的金属工业冶炼方法是A
A.全部采用电解法
B.其中2种采用电解法,另外一种采用热分解法
C.其中一种采用电解法,另外两种采用热还原法
D.全部采用加热分解法
(4)用“大于”“小于”或“等于”填空
| 离子半径 | 还原性 | 得电子能力 |
| N3-大于Al3+ | O2-小于S2- | 35Cl等于37Cl |

A.NH3 B.AlO2- C.CO32- D.CH3COO-
(6)CaCO3和适量HCl溶液反应,当反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得PH变化曲线如图所示.

请用离子方程式表示B-C段发生的反应Ca2++CO32-=CaCO3↓;C点到D点pH增大的原因可用离子方程式表示为CO32-+H2O?HCO3-+OH-.
6.有一在空气中暴露过的NaOH固体,经分析知其含H2O7.65%,含Na2CO34.32%,其余是NaOH.若将ag样品放入bmL1mol/L的盐酸,使其充分作用后,残留酸用25.52mLcmol/L的NaOH溶液恰好中和完全.则蒸发所得溶液,得到固体质量的表达式中(单位为克)( )
| A. | 应含有a | B. | 只含有b | C. | 比含有c | D. | 一定有a、b、c |
7.MOH是强碱溶液与等体积、等浓度的HA弱酸溶液混合后,下列叙述不正确的是( )
| A. | 弱酸的电离常数越小,其所产生的盐水解的程度越大 | |
| B. | 溶液中发生的水解反应是A-+H2O?HA+OH- | |
| C. | 有关离子浓度大小关系是c(M+)>c(A-)>c(OH-)>c(H+) | |
| D. | 该溶液是酸性 |