题目内容
14.A物质为重要的有机化合物,可以发生如下所示的一系列反应.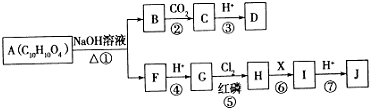
已知:Ⅰ.A分子中苯环上有两个对位的取代基;可以与碳酸氢钠反应生成二氧化碳.
Ⅱ.
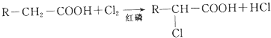
Ⅲ.F的分子式为C3H5O2Na.
请回答下列问题:
(1)可选用氯化铁溶液或浓溴水(填试剂名称)检验C物质中的官能团;J的结构简式为CH2=CHCOOH.
(2)I分子结构中含有碳碳双键,写出⑥的化学方程式
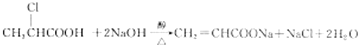 .
.(3)上述流程中属于取代反应的有①⑤(填序号)
(4)J可以发生的反应类型有bc(填序号)
a.消去反应 b.酯化反应 c.加聚反应 d.缩聚反应
(5)写出D聚合的化学方程式为
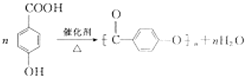 .
.(6)K满足以下条件,则K的结构简式为
 .
.①与A物质互为同系物,且比A分子少一个C原子;
②苯环上两个取代基在对位,能与银氨溶液发生银镜反应;
③相同物质的量的K和A与NaOH溶液反应,消耗NaOH的量相同.
分析 据已知反应①知,A中含有羧基,据已知条件②③,可知F为CH3CH2COONa,A中的对位应为酯基,且是酚羟基与丙酸形成的酯基,则A为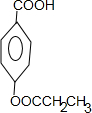 ,A发生碱性水解生成B和F,F酸化得G,则G为CH3CH2COOH,G发生取代反应生成H为CH3CHClCOOH,I分子结构中含有碳碳双键,则H发生消去反应生成I为CH2=CHCOONa,所以试剂X应为氢氧化钠醇溶液,I酸化得J为CH2=CHCOOH;由A的水解的F与B,B为
,A发生碱性水解生成B和F,F酸化得G,则G为CH3CH2COOH,G发生取代反应生成H为CH3CHClCOOH,I分子结构中含有碳碳双键,则H发生消去反应生成I为CH2=CHCOONa,所以试剂X应为氢氧化钠醇溶液,I酸化得J为CH2=CHCOOH;由A的水解的F与B,B为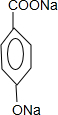 ,其通入二氧化碳时,酚羟基钠反应,羧基钠不反应,C为
,其通入二氧化碳时,酚羟基钠反应,羧基钠不反应,C为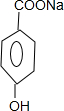 ,D为
,D为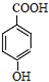 ,据此答题.
,据此答题.
解答 解:据已知反应①知,A中含有羧基,据已知条件②③,可知F为CH3CH2COONa,A中的对位应为酯基,且是酚羟基与丙酸形成的酯基,则A为 ;则G为CH3CH2COOH,H为CH3CHClCOOH,I分子结构中含有碳碳双键,则H发生消去反应生成I为CH2=CHCOONa,所以试剂X应为氢氧化钠醇溶液,I酸化得J为CH2=CHCOOH;由A的水解的F与B,B为
;则G为CH3CH2COOH,H为CH3CHClCOOH,I分子结构中含有碳碳双键,则H发生消去反应生成I为CH2=CHCOONa,所以试剂X应为氢氧化钠醇溶液,I酸化得J为CH2=CHCOOH;由A的水解的F与B,B为 ,其通入二氧化碳时,酚羟基钠反应,羧基钠不反应,C为
,其通入二氧化碳时,酚羟基钠反应,羧基钠不反应,C为 ,D为
,D为 ,
,
(1)C为 ,检验酚羟基可用氯化铁溶液或浓溴水,根据上面的分析可知,J为CH2=CHCOOH,
,检验酚羟基可用氯化铁溶液或浓溴水,根据上面的分析可知,J为CH2=CHCOOH,
故答案为:氯化铁溶液或浓溴水;CH2=CHCOOH;
(2)反应⑥的化学方程式为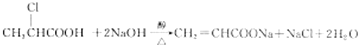 ,
,
故答案为: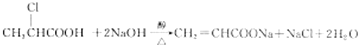 ;
;
(3)根据上面的分析可知,上述流程中属于取代反应的有①⑤,
故答案为:①⑤;
(4)J为CH2=CHCOOH,其中含有的官能团有碳碳双键和羧基,能发生的反应在a、b、c、d中有酯化反应和加聚反应,应选bc,故答案为:bc;
(5)D为 ,D聚合的化学方程式为
,D聚合的化学方程式为 ,
,
故答案为: ;
;
(6)K与A同系物,说明所含官能团相同,能与银氨溶液发生银镜反应,K中有醛基,相同物质的量的K和A与NaOH溶液反应,消耗NaOH的量相同,且两取代基在对位,则K只能是 ,
,
故答案为: .
.
点评 本题考查有机物的推断,是对有机物知识的综合运用,需要学生熟练掌握官能团的性质与转化,注意根据A的分子式及结构特点利用正推法结合反应的条件进行推断,是热点题型,综合考查学生的分析推理能力,难度中等.

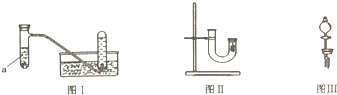
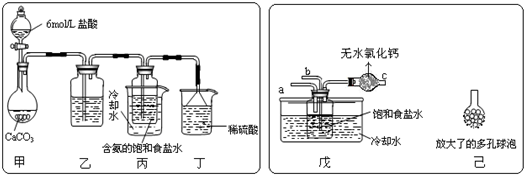
(1)写出试管a中铜与稀硝酸发生反应的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(2)乙同学认为甲虽然收集到的气体为一氧化氮,但并不能说明反应中一定生成一氧化氮.他的理由是在铜和稀硝酸反应容器的上部看到了红棕色气体.
(3)丙同学釆用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮.该同学的步骤如下表所示,请将表格中的实验现象填完整.
| 实验步骤 | 问题 |
| 1.从U型管左端加入稀硝酸直至充满U型管右端 | / |
| 2.用附有铜丝的胶塞塞住U型管右端,观察现象 | U型管右端产生无色气体,溶液变蓝色 |
| 3.待反应停止后打开胶塞,观察实验现象 | 现象是无色气体与空气接触后立即变成红棕色 |
(5)若将32g铜与175mL一定浓度的硝酸巧合完全反应,只产生NO和NO2气体共16.8L(标准状况时体积),该硝酸的物质的量浓度为10mol•L-1.
| A. | 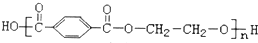 涤纶 涤纶 | B. | 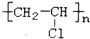 氯纶 氯纶 | ||
| C. | 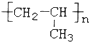 丙纶 丙纶 | D. | 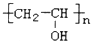 维纶 维纶 |
| A. | 利用太阳能发电 | B. | 用家用汽车代替公交车 | ||
| C. | 利用化石燃料制造燃料电池 | D. | 用节能灯代替白炽灯 |
| A. | CO2的电子式: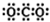 | |
| B. | CS2分子的结构式:S═C═S | |
| C. | S2-的结构示意图: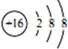 | |
| D. | 8个中子的碳原子的核素符号:${\;}_{8}^{14}$C |
| A. | 轨道表示式表示N2中的共用电子对: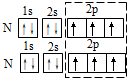 | |
| B. |  只能是氢分子的比例模型 只能是氢分子的比例模型 | |
| C. |  只能是氮分子的球棍模型 只能是氮分子的球棍模型 | |
| D. | CH4分子的比例模型: |
| A. | 维生素C能将+5价砷氧化成As2O3 | |
| B. | 维生素C具有还原性 | |
| C. | 同时大量食用海鲜和青菜过程中+5价砷发生还原反应 | |
| D. | 同时大量食用海鲜和青菜过程中维生素C被氧化 |
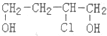 )是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.
)是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂.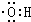 .
.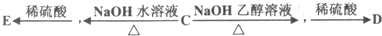
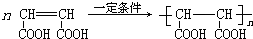 .
.