题目内容
9.能正确表示下列反应的离子方程式是( )| A. | Cl2通入NaOH溶液:Cl2+OH-═Cl-+ClO-+H2O | |
| B. | NaHCO3溶液中加入稀HCl:CO32-+2H+═CO2↑+H2O | |
| C. | 铁锈溶于过量醋酸:Fe2O3+6H+═2Fe3++3H2O | |
| D. | Cu溶于稀HNO3:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
分析 A.离子方程式两边负电荷不相等,违反了电荷守恒;
B.碳酸氢根离子不能拆开,应该保留整体形式;
C.醋酸为弱酸,离子方程式中醋酸不能拆开;
D.铜与稀硝酸反应生成硝酸铜、NO气体和水.
解答 解:A.Cl2通入NaOH溶液,反应生成氯化钠、次氯酸钠和水,正确的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故A错误;
B.NaHCO3溶液中加入稀HCl,碳酸氢根离子不能拆开,正确的离子方程式为:HCO3-+H+═CO2↑+H2O,故B错误;
C.铁锈溶于过量醋酸,醋酸不能拆开,正确的离子方程式为:Fe2O3+6CH3COOH═2Fe3++3H2O+6CH3COO-,故C错误;
D.Cu溶于稀HNO3,反应的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20. 温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.用蒸馏水洗干净滴定管 B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作一次 E.检查滴定管是否漏水
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上
2~3cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)EABCFGD
(2)操作F中应该选择图中乙_滴定管(填标号).
(3)滴定时边滴边摇动锥 形瓶,眼睛应观察B
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化滴定终点溶液颜色的变化是无色变浅红色且半分钟内不褪色
(4)滴定结果如表所示:
滴定中误差较大的是第2次实验,造成这种误差的可能原因是ABD.
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为0.1000mol/L.
(6)如果准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?是(填“是”或“否”).
 温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:A.用蒸馏水洗干净滴定管 B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作一次 E.检查滴定管是否漏水
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上
2~3cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)EABCFGD
(2)操作F中应该选择图中乙_滴定管(填标号).
(3)滴定时边滴边摇动锥 形瓶,眼睛应观察B
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化滴定终点溶液颜色的变化是无色变浅红色且半分钟内不褪色
(4)滴定结果如表所示:
| 滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 1 | 20 | 1.02 | 21.03 | |
| 2 | 20 | 2.00 | 25.00 | |
| 3 | 20 | 0.60 | 20.60 | |
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为0.1000mol/L.
(6)如果准确移取20.00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?是(填“是”或“否”).
17.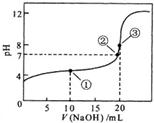 常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000mol/L CH3COOH溶液的滴定曲线如图.下列说法不正确的是( )
常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000mol/L CH3COOH溶液的滴定曲线如图.下列说法不正确的是( )
 常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000mol/L CH3COOH溶液的滴定曲线如图.下列说法不正确的是( )
常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000mol/L CH3COOH溶液的滴定曲线如图.下列说法不正确的是( )| A. | 点①所示溶液中:2c(Na+)=c(CH3COOH)+c(CH3COO-) | |
| B. | 点②所示溶液中:c(Na+)=c(CH3COO-) | |
| C. | 点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
4.化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是( )
| A. | 定性检验SO32-,可用HNO3酸化的BaCl2溶液 | |
| B. | 配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度 | |
| C. | 检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液 | |
| D. | 检验氧化铁中的氧化亚铁,先用硫酸溶液溶解,然后加入盐酸酸化的高锰酸钾溶液 |
14.自然界中存在的元素大多以化合态存在,而我们在生产生活中需许多单质如金属铁、单质氯等.试想,如果把某元素由化合态变为游离态,则它( )
| A. | 一定被氧化 | B. | 一定得到电子 | ||
| C. | 有可能被氧化,也有可能被还原 | D. | 一定由高价变为零价 |
1.物质的量相同的两种气体,在相同条件下,则它们必然( )
| A. | 具有相同数目的原子 | B. | 都占22.4 L | ||
| C. | 具有相同数目的分子 | D. | 具有相同的质量 |
18.在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)?xC(g)△H未知,如图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )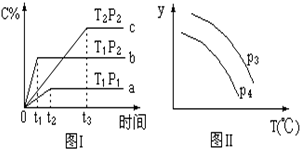

| A. | P3<P4,y轴表示A的转化率 | |
| B. | P3<P4,y轴表示B的体积分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
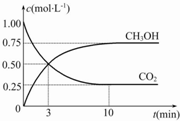 “低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:
“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题: