题目内容
已知A(g)+B(g)═C(g)△H1,D(g)+B(g)═E(g)△H2.若A和D混合气体1mol与B完全反应,反应热为△H3,则A和D物质的量之比为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:在热化学方程式中,化学反应的焓变和方程式的系数之间成正比例,可以根据热化学方程式的意义设未知数来计算.
解答:
解:设A的物质的量是amol,D的物质的量是bmol,则
①a+b=1
②a×△H1+b×△H2=△H3
由方程组解得,则A和D的物质的量之比
=
,
故选B.
①a+b=1
②a×△H1+b×△H2=△H3
由方程组解得,则A和D的物质的量之比
| a |
| b |
| △H3-△H 2 |
| △H1-△H 3 |
故选B.
点评:本题考查了反应热的计算,注意燃烧热为1mol可燃物完全燃烧时生成稳定氧化物的反应热,题目难度不大.

练习册系列答案
相关题目
在一定条件下,下列粒子的还原性顺序为:Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是( )
| A、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| B、I2+SO2+2H2O=4H++SO42-+2I- |
| C、2Fe2++Cl2=2Fe3++2Cl- |
| D、2Br-+4H++SO42-=SO2+Br2+2H2O |
制玻璃、制水泥二种工业生产中,都需要的原料是( )
| A、纯碱 | B、石灰石 | C、石英 | D、黏土 |
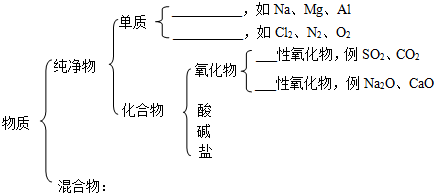
 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
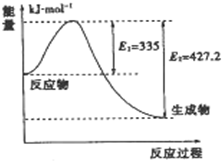
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.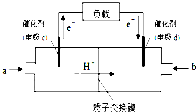

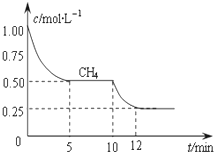 合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生的反应有:
合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生的反应有: