题目内容
下列说法正确的是( )
| A、若2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ?mol-1,则H2燃烧热为241.8 kJ?mol-1 |
| B、原子弹爆炸是放热反应 |
| C、若C(石墨,s)=C(金刚石,s)△H>0,则石墨能量低且键能小 |
| D、由BaSO4(s)+4C(s)=4CO(g)+BaS(s)△H1=+571.2kJ?mol-1① BaSO4(s)+2C(s)=2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1 ② 可得反应C(s)+CO2(g)=2CO(g) 的△H=+172.5kJ?mol-1 |
考点:燃烧热,吸热反应和放热反应,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:A.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量;
B.原子弹爆炸是核裂变;
C.键能越大,键越稳定;
D.依据盖斯定律将方程式变形计算解答.
B.原子弹爆炸是核裂变;
C.键能越大,键越稳定;
D.依据盖斯定律将方程式变形计算解答.
解答:
解:A.水的状态为气态,产物为不是稳定氧化物,△H不代表燃烧热,故A错误;
B.原子弹爆炸属于裂变,不属于化学变化,故B错误;
C.C(石墨,s)=C(金刚石,s)△H>0,石墨键能更大,更稳定,故C错误;
D.依据盖斯定律
,得C(s)+CO2(g)=2CO(g) 的△H=+172.5kJ?mol-1,故D正确;
故选:D.
B.原子弹爆炸属于裂变,不属于化学变化,故B错误;
C.C(石墨,s)=C(金刚石,s)△H>0,石墨键能更大,更稳定,故C错误;
D.依据盖斯定律
| (①-②) |
| 2 |
故选:D.
点评:本题考查了燃烧热、反应热的概念和计算,熟悉概念、盖斯定律的应用是解题关键,题目难度不大,注意核裂变属于物理变化.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列关于蛋白质的叙述中,错误的是( )
| A、蛋白质溶液里加(NH4)2SO4溶液可提纯蛋白质 |
| B、在豆浆中加少量石膏,能使豆浆凝结为豆腐 |
| C、温度越高,酶对某些化学反应的催化效率越高 |
| D、人工合成的具有生命活性的蛋白质--结晶牛胰岛素是我国科学家1965年首次合成的 |
 某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )
某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )| A、活性炭(C) |
| B、磁石(主要成分是Fe3O4) |
| C、铁屑(Fe) |
| D、胆矾(CuSO4?5H2O) |
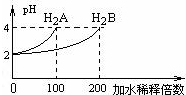 常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述正确的是( )
常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述正确的是( )| A、H2A的电离方程式为H2A═H++HA-,HA-?H++A2- |
| B、pH=4的NaHA水溶液中离子浓度大小为c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-) |
| C、含NaHA、NaHB的混合液离子浓度大小为c(Na+)=c(A2-)+c(HB-)+c(H2B)+c(B2-) |
| D、Na2B的水溶液中,离子浓度大小为c(Na+)>c(B2-)>c(OH-)>c(HB-)>c(H+) |
下列各组物质中,属于同系物的是( )
| A、HCHO、CH3COOH |
B、 、 、 |
| C、CH3COOH、CH3CH2OH |
| D、CH3Cl CH3CH2Cl |
浓硫酸不可以用来干燥的物质( )
| A、N2 |
| B、NH3 |
| C、SO2 |
| D、HCl |
下列关于元素周期表和元素周期律的说法错误的是( )
| A、因为Na比K容易失去电子,所以Na比K的还原性强 |
| B、N与P为同主族元素,且N比P的非金属性强 |
| C、Li、Na、K原子的电子层数随着核电荷数的增加而增多 |
| D、第3周期元素从Na到Cl,非金属性逐渐增强 |
在高温、高压和有催化剂的恒容密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)下列叙述不正确的是( )
| A、若向容器中充入1molN2和3molH2,最终生成2molNH3 |
| B、达到平衡时,体系中各物质的浓度不在改变 |
| C、使用催化剂是为了加快反应速率 |
| D、增大氮气的浓度可加快反应速率 |