题目内容
3.下列物质中含有离子键的是( )| A. | CO2 | B. | NaCl | C. | HCl | D. | CH4 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA族(H元素除外)、第IIA族和第VIA族、第VIIA族元素之间易形成离子键.
解答 解:A.二氧化碳分子中C-O原子之间只存在共价键,为共价化合物,故A错误;
B.NaCl中钠离子和氯离子之间只存在离子键,为离子化合物,故B正确;
C.HCl分子中H-Cl原子之间只存在共价键,为共价化合物,故C错误;
D.甲烷分子中C-H原子之间只存在共价键,为共价化合物,故D错误;
故选B.
点评 本题考查离子键和共价键判断,为高频考点,侧重考查基本概念,明确概念内涵及物质构成微粒是解本题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.如图装置所示的实验中,能达到实验目的是( )
| A. | 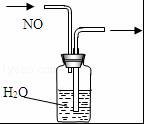 排水集气法收集NO | B. | 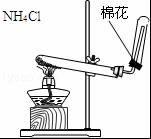 实验室制取氨气 | ||
| C. | 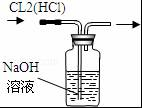 除去氯气中的氯化氢 | D. | 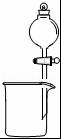 分离碘酒中的碘和酒精 |
14.继屠呦呦从青蒿中成功提取出青蒿素后,中国科学院上海有机化学研究所又在1982年人工合成了青蒿素,其部分合成路线如图所示:下列说法不正确的是( )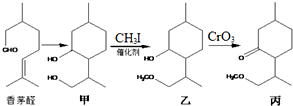

| A. | 香茅醛能发生加聚反应和缩聚反应 | |
| B. | “甲→乙”发生了取代反应 | |
| C. | 甲中不同化学环境的羟基化学性质不同 | |
| D. | 香茅醛存在顺反异构现象 |
8.实验室用锌粒与2mol/L的硫酸制取氢气,下列措施不能增大该反应速率的是( )
| A. | 加水稀释 | B. | 适当增大硫酸浓度 | ||
| C. | 加热 | D. | 用锌粉代替锌粒 |
15.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1mol C12通入足量NaOH溶液中,转移电子数为NA | |
| B. | 18g D2O含有的中子数为10NA | |
| C. | 0.1mol/L的Na2CO3溶液含CO32-数目为0.1NA | |
| D. | 已知白磷(P4)分子结构为正四面体,则1mol P4含共价键数为4NA |
9.《中华人民共和国安全生产法》指出安全生产工作应当以人为本,坚持安全发展、预防为主、综合治理的方针.下列做法不正确的是( )
| A. | 面粉生产车间应严禁烟火 | |
| B. | 含Cl2的尾气用碱溶液处理后再排放 | |
| C. |  天然气运输时应悬挂图所示的标志 | |
| D. | 金属钠失火时应立即用大量冷水扑灭 |
10.T℃时,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),发生反应:2SO2(g)+O2(g)?2SO3(g),5min时甲达到平衡.其起始量及SO2的平衡转化率如表所示.下列叙述不正确的是( )
| 容器 | 甲 | 乙 | 丙 | |
| 起始量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 0~5min内,甲中SO2的反应速率为0.032mol•L-1•min-1 | |
| B. | T℃时,该反应的平衡常数K=400 | |
| C. | 平衡时,SO2的转化率:α1<80%<α2 | |
| D. | 平衡时,丙中气体平均相对分子质量与甲相同 |
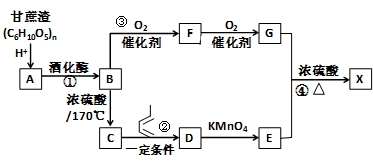

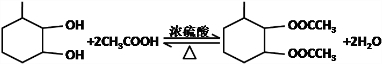 .
.
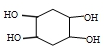 的合成路线为
的合成路线为 .
.