题目内容
有甲、乙、丙三种元素,甲元素第三层的电子数是其第一层的电子数的
,乙元素原子核内无中子,丙元素原子核内有8个质子.
(1)依次写出甲、乙、丙三种元素的元素符号
(2)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式
(3)画出甲元素的原子结构示意图和丙离子的结构示意图 .
| 1 |
| 2 |
(1)依次写出甲、乙、丙三种元素的元素符号
(2)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式
(3)画出甲元素的原子结构示意图和丙离子的结构示意图
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:根据甲元素第三层的电子数是其第一层的电子数的
,第一层为K层,应该含有2个电子,则K层电子数为1,则甲为Na;
乙元素原子核内无中子,元素周期表中只有H无中子,则乙为H元素;丙元素原子核内有8个质子,即其核电荷数为8,则丙为O元素,据此进行解答.
| 1 |
| 2 |
乙元素原子核内无中子,元素周期表中只有H无中子,则乙为H元素;丙元素原子核内有8个质子,即其核电荷数为8,则丙为O元素,据此进行解答.
解答:
解:(1)甲元素第三层的电子数是其第一层电子数的
,第一层为K层,应该含有2个电子,则K层电子数为1,则甲为Na;乙元素原子核内无中子,各元素中只有H无中子,则乙为H元素;丙元素原子核内有8个质子,即其核电荷数为8,则丙为O元素,所以甲乙丙分别为:Na、H、O,
故答案为:甲 Na、乙 H、丙O;
(2)甲、乙、丙三种元素组成的化合物为NaOH,在水中的电离方程式为:NaOH=Na++OH-,
故答案为:NaOH=Na++OH-;
(3)因甲为Na,所以钠的核电荷数=核外电子总数=11,最外层为1个电子,其原子结构示意图为: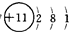 ;
;
氧离子的核电荷数为8,核外电子总数为10,最外层达到8电子稳定结构,氧离子结构示意图为: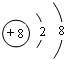 ,
,
故答案为: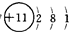 、
、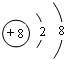 .
.
| 1 |
| 2 |
故答案为:甲 Na、乙 H、丙O;
(2)甲、乙、丙三种元素组成的化合物为NaOH,在水中的电离方程式为:NaOH=Na++OH-,
故答案为:NaOH=Na++OH-;
(3)因甲为Na,所以钠的核电荷数=核外电子总数=11,最外层为1个电子,其原子结构示意图为:
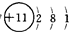 ;
;氧离子的核电荷数为8,核外电子总数为10,最外层达到8电子稳定结构,氧离子结构示意图为:
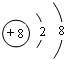 ,
,故答案为:
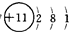 、
、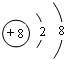 .
.
点评:本题考查位置结构性质的综合应用,题目难度中等,涉及粒子核外电子排布、电子式、电离方程式,正确推断元素的种类为解答该题的关键,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
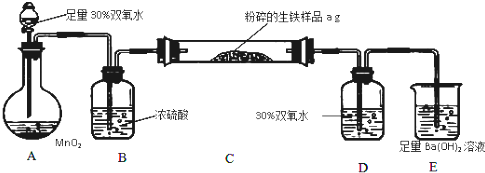

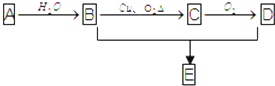
 已知1,2二氯乙烷常温下为无色液体,沸点83.5℃,密度1.23g/mL,难溶于水,易溶于醇、醚、丙酮等有机溶剂.乙醇的沸点为78.5℃.某化学课外活动小组为探究1,2二氯乙烷的消去反应,设计了如下实验装置.请回答下列问题.
已知1,2二氯乙烷常温下为无色液体,沸点83.5℃,密度1.23g/mL,难溶于水,易溶于醇、醚、丙酮等有机溶剂.乙醇的沸点为78.5℃.某化学课外活动小组为探究1,2二氯乙烷的消去反应,设计了如下实验装置.请回答下列问题.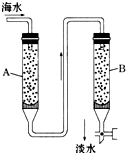 随着现代科学的不断发展,生产和生活所需淡水日益增多,甚至超过人类所能支配的淡水量,使地球上淡水资源发生危机,这就把海水淡化问题提到了科学家的面前.磺化媒(代表式NaR)是一种钠型离子交换树脂,它能使海水中的Ca2+、Mg2+交换除去.
随着现代科学的不断发展,生产和生活所需淡水日益增多,甚至超过人类所能支配的淡水量,使地球上淡水资源发生危机,这就把海水淡化问题提到了科学家的面前.磺化媒(代表式NaR)是一种钠型离子交换树脂,它能使海水中的Ca2+、Mg2+交换除去.