题目内容
下列有关热化学方程式的叙述正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1,则氢气的燃烧热为285.8kJ?mol-1 |
| B、已知C(石墨,s)═C(金刚石,s);△H>0,则石墨比金刚石稳定 |
| C、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.4kJ?mol-1 |
| D、已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
考点:热化学方程式
专题:化学反应中的能量变化
分析:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量分析判断;
B、物质能量越高越活泼;
C、醋酸是弱酸操作电离平衡,电离过程是吸热反应;
D、一氧化碳燃烧生成二氧化碳过程是放热反应,放热反应焓变为负值;
B、物质能量越高越活泼;
C、醋酸是弱酸操作电离平衡,电离过程是吸热反应;
D、一氧化碳燃烧生成二氧化碳过程是放热反应,放热反应焓变为负值;
解答:
解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量分析判断,已知2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1,则氢气的燃烧热为285.8kJ?mol-1,故A正确;
B、物质能量越高越活泼,已知C(石墨,s)═C(金刚石,s);△H>0,金刚石能量高于石墨,则石墨比金刚石稳定,故B正确;
C、含20.0g NaOH的稀溶液中含有溶质0.5mol,与稀盐酸完全中和,放出28.7kJ的热量,中和热为57.4KJ/mol;醋酸是弱酸操作电离平衡,电离过程是吸热反应,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H>-57.4kJ?mol-1,故C错误;
D、一氧化碳燃烧生成二氧化碳过程是放热反应,放热反应焓变为负值,已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1<△H2,故D错误;
故选AB.
B、物质能量越高越活泼,已知C(石墨,s)═C(金刚石,s);△H>0,金刚石能量高于石墨,则石墨比金刚石稳定,故B正确;
C、含20.0g NaOH的稀溶液中含有溶质0.5mol,与稀盐酸完全中和,放出28.7kJ的热量,中和热为57.4KJ/mol;醋酸是弱酸操作电离平衡,电离过程是吸热反应,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H>-57.4kJ?mol-1,故C错误;
D、一氧化碳燃烧生成二氧化碳过程是放热反应,放热反应焓变为负值,已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1<△H2,故D错误;
故选AB.
点评:本题考查了热化学方程式书写,燃烧热,中和热概念的分析应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
已知某元素R的气态氢化物的化学式为H2R,下列叙述中不正确的是( )
| A、该元素的原子最外电子层上有6个电子 |
| B、该元素的原子高正价氧化物的化学式为RO2 |
| C、该元素一定是非金属元素 |
| D、该元素最高价氧化物对应的水化物的化学式为H2RO4 |
下列有关NA的说法不正确的是( )
| A、标况下1mol HF 的体积约为22.4 L |
| B、1.44g CaO2中所含阴离子数目为0.02NA |
| C、标况下4.48L CO2中含有的共用电子对数目为0.8NA |
| D、标准状况下,11.2L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA |
常温下,下列离子或分子在指定溶液中能大量共存的一组是( )
| A、FeCl3饱和溶液:K+、I-、Cl-、H+ |
| B、使紫色石蕊试液变蓝色的溶液:Na+、NO3-、Br-、NH3?H2O |
| C、pH=1的溶液:Cr2O72-、K+、NO3-、C2H5OH |
| D、能溶解Al2O3的溶液:Na+、Mg2+、HCO3-、Cl- |
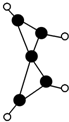 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示,下列说法中不正确的是( )| A、该分子的分子式为C5H4 |
| B、该分子中碳原子的化学环境有2种 |
| C、1mol X在一定条件下可与2mol H2发生反应 |
| D、该分子中只有C-C键,没有C═C键 |
下列有关叙述正确的是( )
| A、元素性质呈周期性变化的根本原因是元素化合价呈周期性变化 |
| B、BF3和CO2分子中所有原子均满足最外层为8电子结构 |
| C、已知114号元素的一种核素的质量数为298,则该元素的相对原子质量为298 |
| D、[14NH3T]+ 中,电子数、质子数、中子数之比为10:11:9 |
 炭雕(如图所示)是一种集观赏与空气净化为一体的产品,这种产品可对车内及室内空气中的一氧化碳、苯、甲醛、烟雾等有害气体进行有效吸附.取一块制作炭雕的下脚料,进行下面的实验.下列有关叙述不正确的是( )
炭雕(如图所示)是一种集观赏与空气净化为一体的产品,这种产品可对车内及室内空气中的一氧化碳、苯、甲醛、烟雾等有害气体进行有效吸附.取一块制作炭雕的下脚料,进行下面的实验.下列有关叙述不正确的是( )| A、将炭雕下脚料在空气中点燃,可以得到使澄清石灰水变浑浊的气体 |
| B、将炭雕下脚料研成粉末,加入到稀的红墨水中,红墨水褪色 |
| C、将炭雕下脚料研成粉末,与氧化铜粉末混合加热,可以得到红色固体 |
| D、将炭雕下脚料加入到盛有氯气的集气瓶中,静置一段时间,黄绿色变浅,其原因是炭雕下脚料中的物质与氯气发生氧化还原反应 |
25℃时,a mol?L-1 HCl溶液与b mol?L-1一元碱BOH等体积混合后,pH为7,则下列关系可能正确的是( )
| A、a>b |
| B、a<b |
| C、c(Cl-)>c(B+) |
| D、c(Cl-)<c(B+) |
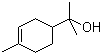 )的分子式为
)的分子式为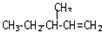 一定条件发生加聚反应时的化学方程式
一定条件发生加聚反应时的化学方程式